
时间:2026-02-06浏览次数:311
最早一项研究采用人回肠组织干细胞来源的类器官模拟药物性腹泻,并对31种药物进行验证。该方法在预测药物性腹泻临床发生率方面具有90%的准确率。
(doi: 10.1016/j.tiv.2020.104928.)
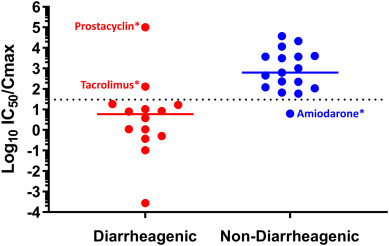
后续研究利用组织干细胞来源的小肠和结肠类器官探索了胃肠道毒性的分子决定因素,深入解析了多柔比星和吉非替尼诱导副作用的作用机制。
(doi: 10.3390/ijms23031286;
doi: 10.3390/ijms23042213.)
研究人员开发出一种经济高效的肠道类器官培养方法,实现了小分子化合物的表型高通量筛选。通过该平台,未分化的类器官能精准区分具有细胞毒性或非细胞毒性的化合物。更有意思的是利用该平台对人类、大鼠和犬类类器官的化合物反应进行比较时,发现化合物的物种特异性敏感性差异与临床前研究结果高度吻合,充分证明了类器官在早期安全性评估中的应用价值。
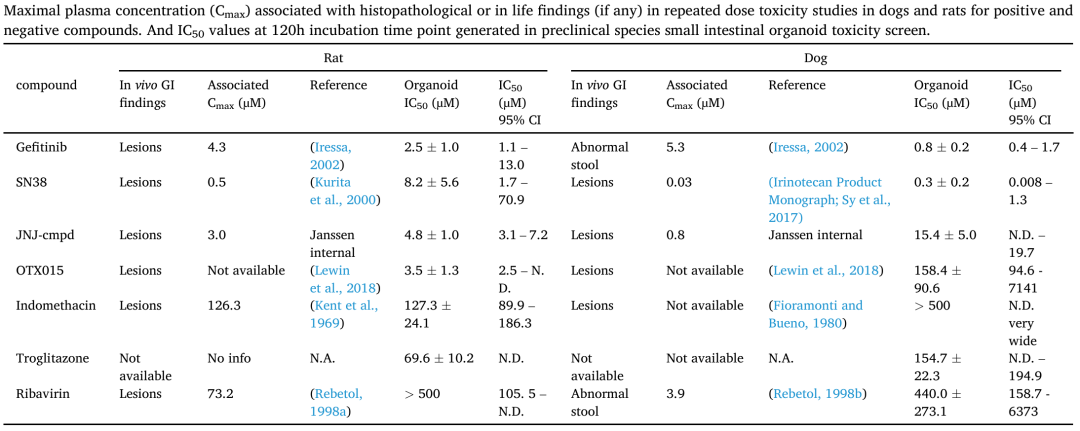
肠道类器官平台还被用于评估靶向蛋白生物制剂(如靶向细胞生物制剂TCBs)的“靶向肿瘤外效应”,包括避免临床前研究中出现的跨物种交叉反应问题。通过补充免疫细胞的肠道类器官和肿瘤类器官模型证实肿瘤细胞杀伤剂(TCBs)具有组织特异性肿瘤外毒性,成功识别了传统基于组织的模型(缺乏这些免疫成分)无法预测的临床不良反应。
( doi: 10.1038/s41551-023-01156-5)
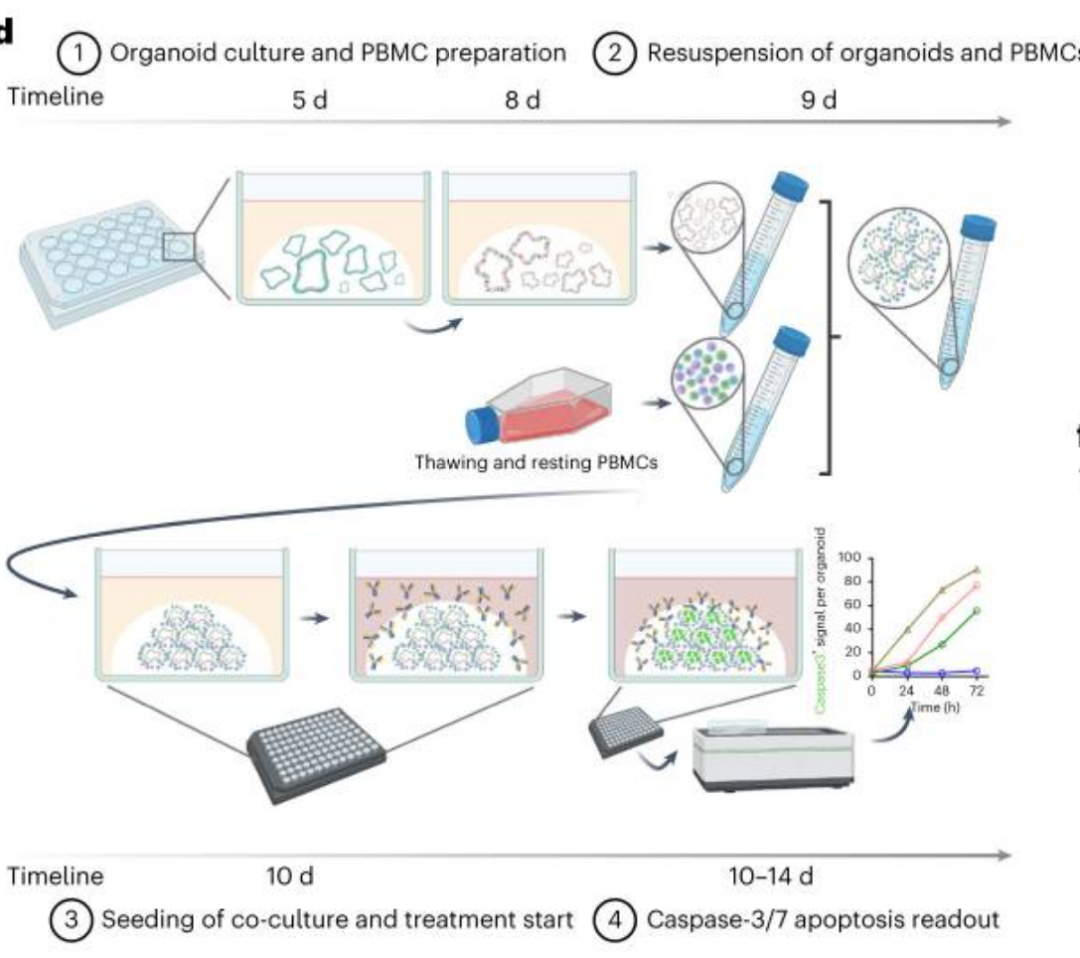
研究人员还通过整合上皮类器官与自体组织驻留记忆(TRM)T细胞构建了人类肠道免疫类器官,并将其用于研究癌症患者中观察到的TCBs诱导的肠道炎症。
(doi: 10.1038/s41586-024-07791-5)
下一篇:药物神经毒性评价
