
时间:2026-01-12浏览次数:538
肝癌在各类致死癌症中位居第四位,是我国第六大常见癌症疾病。我国肝癌的发病率位居世界前列,患者预后效果差且致死率高。肝癌治疗一般以手术切除和化疗联合为主,多数患者由于其发现病症时已经处于肝癌中晚期,治疗效果并不理想。近年来,尽管肝癌治疗方式不断完善,如手术、微创介入、免疫、靶向治疗等,患者5年生存率有了一定提高,但整体治疗效果仍不理想。因此,开发新型抗肿瘤药物以及个体化药物迫在眉睫,而抗肿瘤药物从研发到临床应用肿瘤模型的选择至关重要。
肝癌研究的传统模型包括体内模型和体外模型两种,由于肝脏疾病存在明显的异质性,而传统肝癌研究模型对于细胞真实形态、空间结构和细胞微环境无法完全准确反映及表达,故研究结果无法应用到临床实践;动物模型的种属差异性限制了其在临床研究的延续性。致力于反映人体真实情况的肝癌模型是研究者梦寐以求的目标,类器官作为一种新型体外模型,不仅弥补了传统模型不准确、不全面、不稳定的缺点,还为肝癌免疫研究和血管生成等微环境研究提供了可能性,并可用于高通量药物筛选和生物样本库的构建。类器官模型将在精准治疗与再生医学方面提供更大的潜力。
类器官是指由干细胞或器官祖细胞以一种类似体内细胞分化的形式组织成器官特异性的细胞集合。Nuciforo等对于类器官的定义主要有3个基本要求。首先要有一个以上的器官细胞类型;其次需具备该器官的一些功能;最后具有该器官的相对应空间结构。Huch等对类器官提出了一个可能更准确的概念,将类器官定义为一群来自体外的3D细胞群,并且如果是来自于组织的干细胞或者多能干细胞(PSC),还具有自我更新和组织的功能,最终呈现出具有原始器官结构和功能的细胞体系。肿瘤类器官是一种恶性细胞团,且可利用原代恶性细胞保留原代肿瘤的病理学形态特征、基因组与转录组特征、药物敏感性及恶性细胞间异质性,还可以持续增殖。
机体内细胞处于一个十分复杂的微环境,会受到各种调控,包括细胞内和细胞外的一些化学信号、物理信号,而细胞外基质是这些信号相互作用的关键区域。理想的肿瘤模型应能在体外重现体内肿瘤的特征,比如一些基因组特征、组织学形态特点、恶性细胞间异质性及肿瘤微环境。在传统的培养模型中,仅能构建出单维度细胞间的联系,而类器官的培养则可有类似体内组织器官的相互作用。目前研究构建出胃、脑、肝脏等多种体外类器官。类器官模拟肿瘤等疾病的发生发展相关研究和类器官药物敏感性的检测研究越来越引起学者高度重视。
类器官所建立的环境复杂且具有生理生物学特征,会影响到诸如细胞形态、活性、细胞增殖与迁移等多个方面。研究表明,如果可将多能干细胞诱导并且分化成器官祖细胞,那么原则上就可以产生相应的类器官。但目前该模型依然存在不足,如无法完全重现体内肿瘤微环境,使其在临床方面的应用仍然受限。
肝细胞癌类器官构建实验步骤
1. 将移液枪头置于冰上预冷,将基质凝胶在冰上或4°C下解冻,并将24孔细胞培养板预热至37°C。
2. 收集处于对数生长期的HepG2细胞,用PBS轻轻冲洗,并用胰酶消化细胞。
3. 消化后,制备并收集单细胞悬浮液,以1500转/分钟的速度离心3分钟,弃去上清液,并将细胞在DMEM完全培养基中重悬,调整细胞浓度至1.0×10^6细胞/毫升。
4. 细胞接种:在冰上将解冻的基质凝胶与调整浓度的单细胞悬浮液按1:1比例混合,轻轻吹打混合。使用预冷的200μL移液枪头,将40-50μL混合单细胞悬浮液垂直滴入预冷的24孔板中,形成拱形的细胞滴。
5. 在37°C、5% CO2饱和湿度的细胞培养箱中稳定30分钟后,向每个孔中加入500-2mL肝细胞癌类器官完全培养基,继续培养。
6. 每天观察并拍照记录,大约5-7天后可以观察到均匀的肝细胞癌类器官。
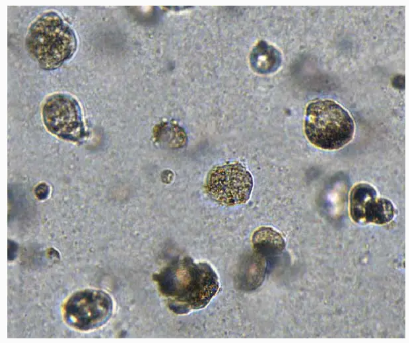
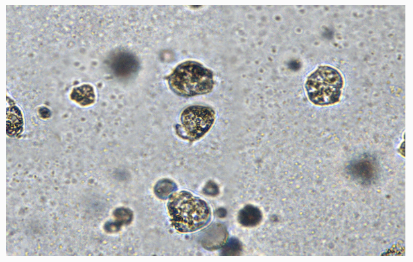
培养5天后来自HepG2细胞系的类器官培养结果。
常见问题解答
1. 在处理基质凝胶时应采取哪些预防措施?
所有操作应在无菌环境中进行,使用预冷的移液管以确保基质凝胶呈均匀的糊状。
2. 如何分装、冷冻和使用基质凝胶?
解冻后,Arcegel基质凝胶可以分装到多个小管中,所有分装都应使用预冷的冷冻管,快速冷冻并储存,以避免反复冻融。
3. 在不同孔板中培养类器官需要多少体积的基质凝胶和培养基?
类器官通常在24孔板中以50μl/滴的基质凝胶进行培养,然后加入500~800μl的培养基覆盖滴液。在96孔板中,使用10μl/滴的基质凝胶,然后加入200μl的培养基覆盖滴液。在6孔板中,每个孔可以接种多个50μl的滴液,然后加入2~3ml的培养基覆盖滴液。
肝癌类器官的应用
1. 药物筛选
药物筛选是新药研发的关键步骤,而类器官具有稳定的基因组,更接近人体细胞的生理状态并且更适合于生物转染和高通量筛选。此外,类器官不仅可以用于药物研发阶段,还可以用于临床前试药,通过对患者来源类器官的分析,能够了解遗传学变化的原因,为后续治疗提供数据支撑。Li等用肝癌类器官进行药物筛选,从胆管癌手术标本不同位置取材,构建27个肝癌类器官细胞株并用129种抗肿瘤药物进行筛选,最后仅有一小部分药物广泛有效,表明应用肝癌类器官可以达到筛选药物的作用。由于肝脏是负责药物代谢的主要器官,肝脏类器官也被用于研究治疗带来的潜在副作用。
2. 疾病建模
由于类器官可以高度模拟组织的生理结构、功能以及发育和分化的过程,不仅可用于研究肝脏肿瘤的起始,还可以研究肝脏肿瘤的微环境,因此肝癌类器官可以作为一种良好的体外预测模型。通过建立类器官生物库,将患者肿瘤特征与生物库中的类器官进行对比,从而为患者选择更为精准的治疗方案。
3. 再生医学
肝移植是治疗肝纤维化、肝癌等疾病最有效的方法之一,但适合进行移植的组织缺乏,导致肝移植存在一定局限性,而肝脏类器官的出现为此提供了一种可能性。有学者对肝脏类器官培养体系进行了改进,使其存活率大大增加,还能够分泌更多的白蛋白。Sampaziotis等建立的不同胆囊区域(肝内胆管、胆总管和胆囊)类器官模型的效果良好,修复了人类肝脏的胆管系统,为临床研究提供了实验基础。
4. 个性化医疗
个性化医疗也称为精准医疗。肿瘤具有异质性,从而导致个体差异显著,对肿瘤药物的研究难点亦在于此。肝癌类器官较好地解决了该问题,在肝癌类器官培养过程中保存了原始肿瘤基因的特征,故而对临床肿瘤样本进行取样与诱导形成具有该患者肿瘤特征的肝癌类器官,对后续研究与治疗都更为便利。将类器官应用于肝癌研究的另一个前沿方向是使用从类器官收集的组学分析来间接指导临床用药,通过RNA测序还有代谢组学的分析,可推测药物对肝癌细胞系的生长是否起到抑制作用,为药物疗效的评价提供依据。
5 生物标志物
通过分子分析方法,包括蛋白质组学、代谢组学、转录组学,能够发现一些关键的生物标志物,可对辅助诊断和精准医疗起到重要作用。胰腺和结直肠癌患者来源的类器官已经通过组学分析,将遗传、转录信息与药物作用建立了联系,但是肝脏类器官由于样本量小而尚未建立。
