【五分钟讲实验】生物相容性试验案例详解分析!
时间:2024-04-02 阅读:1455生物相容性是指生物材料在机体特定部位产生各种复杂的生物、物理、化学的反应,即某些材料或者药物与人体接触或者植入体内是否能够“兼容”,会不会对我们的人体产生伤害。其测试项目比较多,主要有细胞毒性、致敏、刺激、全身毒性(急性毒性)、亚慢性毒性(亚急性毒性)、遗传毒性、植入、慢性毒性、致癌性、生殖和发育毒性和生物降解等。
ISO10993标准通常包括的测试项目有体外细胞毒性测试、皮肤刺激性测试、致敏试验,也称生物学评价的基础三项:
细胞毒性:将样品的浸提液放入生长旺盛的细胞悬液中培养,观察细胞形态。(GB/T 16886.5-2003、ISO 10993-5-1999)
皮肤刺激:将样品的浸提液滴到吸收性纱布或者直接将凝胶材料,敷贴于动物去毛后的背部两侧,观察部位情况。(GB/T 16886.10-2005 ISO、10993-10)
致敏试验:将样品浸提液进行皮内注射到动物皮肤,后续通过凝胶材料敷贴于动物去毛后的背部,经过诱导和激发,对相应部位进行观察。(GB/T 16886.10-2005、ISO 10993-10)
1. 细胞
小鼠成纤维细胞L929、NIH3T3;人正常肝细胞LO2。
2. 浸提液制备
凝胶材料+培养基,37℃,72h,0.22um过滤后备用。
3. 细胞分组(n=3)
① 正常细胞
② 正常细胞+浸提液浓度A
③ 正常细胞+浸提液浓度B
④ 正常细胞+浸提液浓度C
干预时间:24h、48h、72h;CCK-8检测细胞毒性。
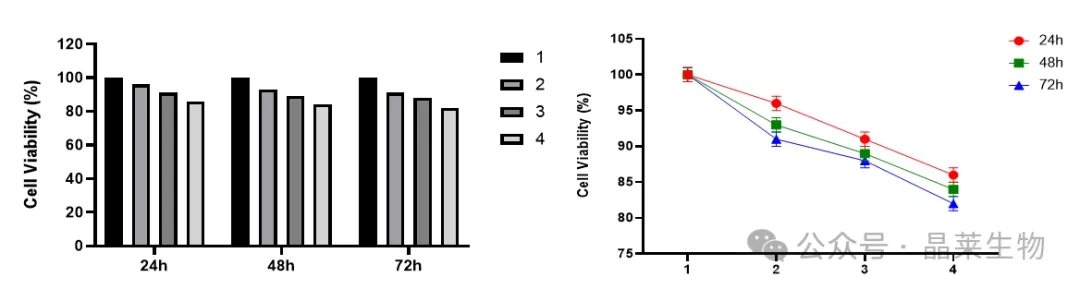
1. 材料准备
① 实验动物:兔。
② 其他材料:凝胶、浸提液(凝胶材料+培养基,37℃,72h,0.22um过滤后,滴于纱布上备用)。
2. 造模方法
① 背部脊柱两侧区域去毛,在左侧脱毛区进行凝胶/浸提液孵育,右侧脱毛区涂抹溶媒/赋形剂,绷带包扎固定后4h去除药物,温水洗净,
② 观察皮肤反应,根据红斑及水肿反应进行计分。
③ 此后于同一时间、同一方法进行处理,连续7天,观察皮肤反应并计分。
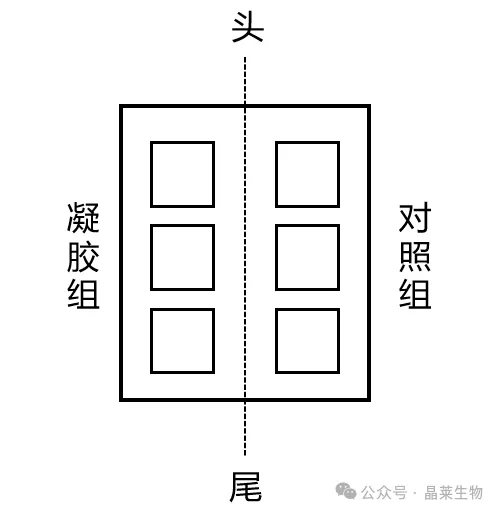
3. 参照《GB/T16886第10部分:刺激与皮肤致敏试验》评价标准:
① 每组的初级刺激分数为每组实验分数之和除以观察到的测试点数;
② 每只动物原发性刺激计分是材料组减去对照组的初级刺激评分;
③ 原发性刺激指数(Primarily Stimulation Index,PII)是每只动物的原发性刺激评分除以动物总数。
4. 判断刺激反应类型

① PII在0.0~0.4为轻微反应;
② 0.5~1.9为轻度反应;
③ 2.0~4.9为中度反应;
④ 5.0~8.0为重度反应。
1. 材料准备
① 动物:豚鼠
② 药物:浸提液(凝胶材料+培养基,37℃,72h,0.22um过滤后备用)、弗氏完全佐剂、阳性对照(5%甲醛)、阴性对照(生理盐水)。
2. 造模方法(皮内与涂皮相结合方式)

① 皮内诱导:将豚鼠随机分成3组,分别为试验组、阴性对照组和阳性对照组,每组6只。实验前24h将豚鼠背部区域去毛,以脊柱为对称,左右两边各设置3个注射点,每点均为皮内注射,注射剂量0.1mL。从上至下分别注射A、B、C三种不同溶液:
试验组 (A)弗氏完全佐剂/生理盐水 1:1
(B)凝胶浸提液
(C)A液/B液 1:1
阳性对照组 (A)弗氏完全佐剂/生理盐水 1:1
(B)5%甲醛溶液
(C)A液/B液 1:1
阴性对照组 (A)弗氏完全佐剂/生理盐水 1:1
(B)生理盐水
(C)A液/B液 1:1
注射7天后进入局部诱导阶段。
② 局部诱导:敷贴前24h,背部再次去毛,皮肤消毒,用10%SDS进行按摩处理,导入皮肤。第二天,将浸泡有凝胶浸提液、生理盐水和5%甲醛溶液的纱布分别贴敷于试验组、阴性对照组、阳性对照组动物背部试验区,绷带包扎固定,48h后除去绷带和纱布,14天后进入激发阶段。
③ 激发阶段:将纱布置于凝胶浸提液、阴性对照液和阳性对照液中浸透,剃除动物腹部毛发进行敷贴,绷带包扎固定,24 h后除去绷带和纱布。随后观察24 h、48 h每组动物的腹部激发部位皮肤变化情况。
3. Magnusson和Kligman分级标准:

① 当阴性对照组动物评分小于1分,而试验组动物皮肤评分大于或等于1分时,表明发生致敏。
② 如果阴性对照组动物的评分大于或等于1,且实验组动物的反应超过阴性对照组中最强的反应,则表明发生了致敏。
③ 有时试验组有反应的动物多于对照组,但反应强度不超过对照组的反应强度,在这种情况下,需要在初次致敏后1至2周进行第二次注射,以明确致敏原因。使用的方法与第一次感染相同,使用动物未测试的一侧。
1. 材料准备
① 样本:人新鲜抗凝全血
② 药物:浸提液(凝胶材料+培养基,37℃,72h,0.22um过滤后备用)、PBS、 TritonX-100。
2. 检测方法
①准备人枸橼酸抗凝全血(9:1,全血:3.2%枸橼酸钠抗凝剂);
②抗凝全血 1000 rpm 离心 10 分钟,取下层红细胞层加入等体积 PBS混匀;
③ 1000 rpm 离心 10 分钟,取下层红细胞用 PBS 稀释至 5%;
④取 6mL浸提液、PBS(阴性对照)、0.1% TritonX-100(PBS稀释,阳性对照),分别加入4mL 红细胞稀释液,轻轻混匀;
⑤37 ℃放置 1小时后,3000 rpm离心 10分钟;
⑥于 540 nm 处测上清吸光度。

3. 溶血率计算公式
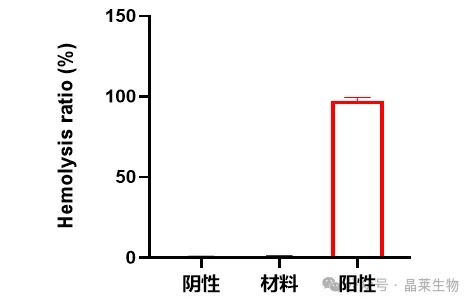
Hemolysis ratio (%) = [(As− A0) ⁄(Ap− A0)] × 100%
As是各组的吸光度,A0是空白对照组的吸光度,Ap是阳性对照组的吸光度。
1. 实验材料
① 动物:SD大鼠。
② 药物:凝胶。
2. 造模方法
大鼠麻醉后,将凝胶植入大鼠的背部肌肉。在0、7、14天处死大鼠,取凝胶周围组织固定48h后,脱水包埋,石蜡切片,进行HE染色。
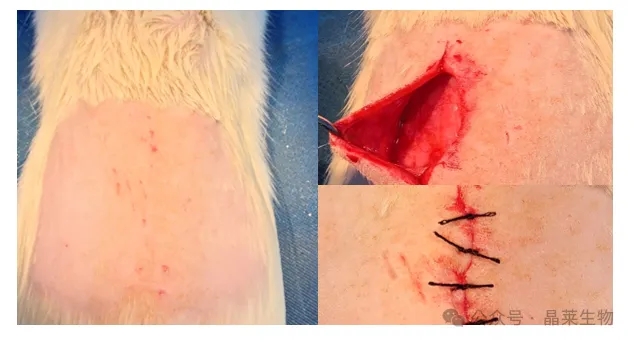
(体内免疫相容性可选:IHC检测CD68表达)
3. 病理分析
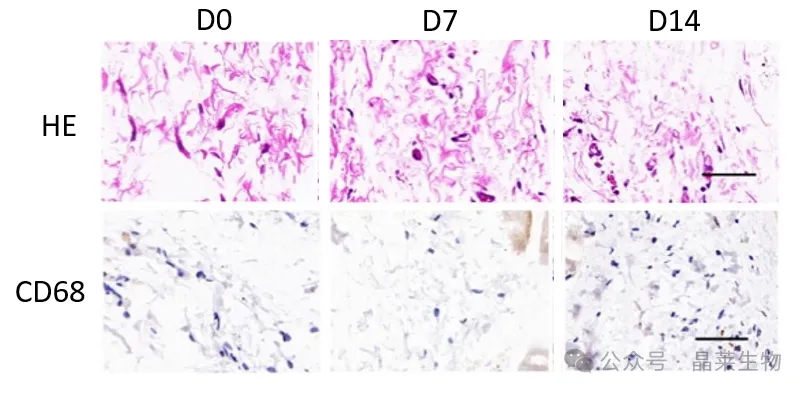
① HE染色如未见明显细胞浸润,则说明材料具有较好的组织相容性。
② IHC染色如CD68 阳性数量与对照组相比无显著差异,则说明材料不会促发炎症,具有良好的体内免疫相容性。
目前对凝胶材料的生物相容性研究涉及医学、药学、生物工程等多个领域:
1. 医用生物材料: 在医学领域,凝胶材料广泛应用于组织工程、修复和再生等方面,生物相容性是评估这些凝胶材料在与生物体接触时是否引起毒性或免疫反应的重要指标。
2. 药物传递系统: 凝胶材料可作为药物传递系统的载体,用于控制释放药物并提高药物的生物利用度,此时其生物相容性研究有助于评估凝胶材料对药物和生物组织的相互作用。
3. 手术辅助材料: 在外科手术中,凝胶材料也常用于辅助修复和重建组织,如止血、伤口封闭、软组织修复等。其生物相容性研究有助于评估相关产品在手术过程中的安全性和有效性。
晶莱生物
以上部分数据与结果图来源于网络和文献,如有侵权请联系客服删除。

我司提供一站化凝胶材料生物相容性研究服务,一份材料,十分靠谱!
关于晶莱
关注公众号,了解更多!