
时间:2021-09-23浏览次数:8822

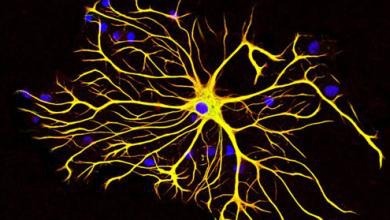
实验技术简介:
体外神经细胞的培养已成为神经生物学研究中十分有用的技术手段。
神经细胞培养的主要优点:
(1)分散培养的神经细胞在体外生长成熟后,能保持结构和功能上的某些特点, 而且长期培养能形成髓鞘和建立突触联系,这就提 供了体内生长过程在体外重现的机会。
(2)能在较长时间内直接观察活细胞的生长、分化、形态和功能变化,便于使用各种不同的技术方法如相差显微镜、荧光显 微镜、电子显微镜、激光共聚焦显微镜、同位素标记、原位杂交、免疫组化和电生理等手段进行研究。
(3)易于施行物理(如缺血、缺氧)、化学和生物因子(如 神经营养因子)等实验条件, 观察条件变更对神经细胞的直接或间接作用。
(4)便于从细胞和分子水平探讨某些神经疾病的发病机制,药物或各种因素对胚胎或 新生动物神经细胞在生长、发育和分化等各方面的影响。
一、液体配制:硼酸硼砂缓冲液:0.05M四硼化钠45ml,0.2M硼酸55ml,pH8.4;胰酶-EDTA消化液:胰酶-0.125g;EDTA-0.2g;D-Hanks平衡盐液定容至100ml。所用的培养板、培养瓶或玻片预先经100μg/L多聚赖氨酸硼酸盐缓冲液于37℃包被4h,三蒸水洗三遍晾干备用。
二、操作步骤如下:
1、出生2 d SD大鼠麻醉后,碘酒、75%乙醇消毒腹部皮肤,依次剪开皮肤、肌肉、皮下筋膜,无菌操作下取出胚胎放入预冷的D-Hanks平衡盐液中。
2、在解剖显微镜下分离并取出胚胎大脑皮层,除去脑膜,剪碎组织成约1mm3大小,加入胰酶-EDTA消化液并放入37℃孵箱内消化20min,中间摇晃一次。
3、随后用滴管吸出组织转移到装有预冷的培养液(DMEM+10%FBS)的离心管内终止消化液作用5min。
4、用滴管吸出组织转移到装有预冷的DMEM+10%FBS的离心管内,用火焰抛光的巴斯德滴管吹打数次,静置后取上清吸到另一支离心管内。重复上述步骤2~3次。
5、将所收集的上清经200目筛网过滤。
6、过滤后的细胞悬液于800r/min离心5min,弃上清,管内加入新鲜培养液(DMEM+20%FBS)并吹打成单细胞悬液。
7、细胞计数,调整细胞密度按1.5×105/cm2种入6孔板内,放入CO2孵箱中培养。培养48h后换液并加入Ara-C使其终浓度为1×10-5mM/L。Ara-C作用24h后全量换液。以后每隔3天半量换液一次。
三、无菌操作的注意事项:
细胞原代培养一定要保持工作区的无菌清洁,先用紫外灯杀菌1h,操作前用75%乙醇消毒,穿上实验服,戴上口罩和帽子,操作时不能大声说话,双手戴上一次性橡胶手套,整个无菌操作都应该在酒精灯的周围进行。
四、服务流程:
1、 讨论分析实验方案
2、 确定服务内容
3、 签订服务合同
4、 进行实验,定期向客户反馈
5、 整理实验报告
6、 完成合同内容
7、 后续实验服务,进一步合作
五、细胞服务项目: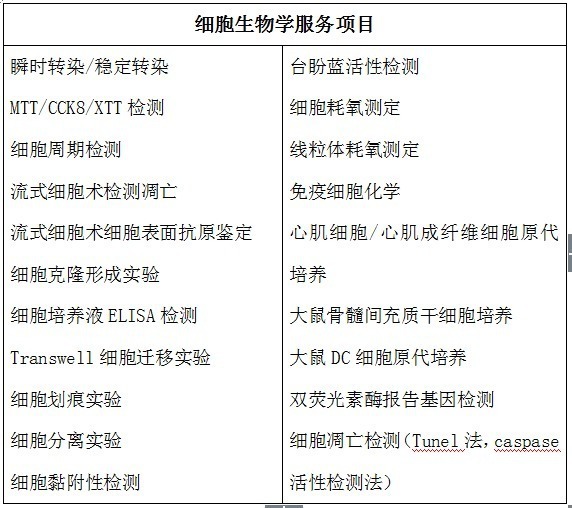
做实验,找晶莱!您的科研生涯,我们一路相伴!
【平台项目开展范围】慢病毒,腺病毒,RNAi类,分子生物实验,病理实验,免疫学实验,细胞实验,动物实验,蛋白组学实验,芯片类实验,并为广大客户朋友们提供课题设计指导、基金申请指导等服务。
晶莱生物服务流程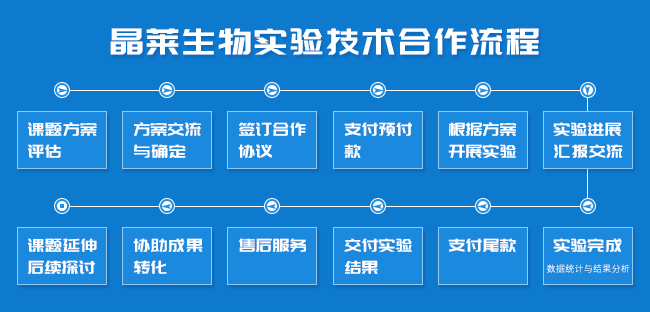
晶莱生物实验服务项目
| 动物实验 | 细胞生物学 | 病理实验 |
| 消化系统模型 | 细胞培养 | 病理染色 |
| 胃酸分泌模型 | 普通细胞株 | HE染色 |
| 脓毒症模型 | 细胞缺氧培养 | 油红O染色 |
| 胃溃疡模型 | 细胞培养+支架 | 番红固绿染色 |
| 胰腺炎模型 | 干细胞培养 | Masson染色 |
| 肝纤维化模型 | 原代细胞分离/提取/培养 | 天狼猩红染色 |
| DIO肥胖模型 | 细胞转染/病毒感染 | PAS糖原染色 |
| 胆结石模型 | Trans well共培养 | 阿利新蓝染色 |
| 结肠炎(UC)模型 | 细胞增殖 | 甲苯胺蓝染色 |
| 脂肪肝模型 | 细胞计数 | 尼氏染色 |
| 急性肝损伤模型 | 生长曲线测定 | LFB髓鞘染色 |
| 免疫、代谢系统疾病模型 | 存活曲线测定 | 普鲁士蓝染色 |
| 骨质疏松模型 | ccK-8增殖检测 | VG染色 |
| 糖尿病模型 | MTT增殖检测 | EVG染色 |
| 高尿酸血症模型 | CFSE检测增殖-流式检测 | VonKossa染色 |
| 呼吸系统模型 | BrDU检测-免疫荧光法 | 刚果红染色 |
| 肺纤维化模型 | 细胞凋亡 | 苏丹黑B染色 |
| 慢性肺阻塞模型 | Annexin V/PI流式检测细胞凋亡 | Trap染色 |
| 急性肺损伤模型 | WB检测凋亡相关蛋白 | 抗酸染色 |
| 哮喘模型 | 透射电镜观察凋亡小体 | 革兰氏染色 |
| 肺栓塞模型 | Tunel染色(POD法,DAB显色) | AB-PAS染色 |
| 支气管炎模型 | Tunel(荧光法,含试剂盒) | 亚甲基蓝染色 |
| 泌尿生殖系统模型 | DNA ladder法 | 苯胺蓝染色 |
| 慢性肾衰模型 | 细胞周期 | 荧光 DAPI染色 |
| 急性肾衰模型 | 细胞显微计数 | 普鲁士蓝染色 |
| 肾间质纤维化模型 | PI染色 | 间苯二酚碱性品红染色 |
| 肾结石模型 | BrdU渗入法 | 银染 |
| 肾炎模型 | 免疫荧光染色 | 黑色素染色 |
| 子宫内膜异位症模型 | PI流式检测细胞周期 | 镀银染色 |
| 心血管系统模型 | 细胞运动 | PASM 六胺银染色 |
| 冠心病模型 | Transwell检测细胞迁移 | VG染色 |
| 心肌梗死模型 | Transwell检测细胞侵袭 | 富尔根染色 |
| 心脏骤停模型 | 细胞划痕 | 亚甲基蓝染色 |
| 慢性心力衰竭模型 | 细胞克隆 | 碘-碘化钾染色 |
| 动脉粥样硬化模型 | 集落形成法/稀释铺板方法 | Goldner三色法染色 |
| 白血病模型 | 软琼脂克隆法 | PAS-萘酚磺S染色 |
| 高血压模型 | 毛细管克隆法 | 改良苯酚品红染色 |
| 神经系统模型 | 体外实验血管生成 | 网状纤维染色 |
| 脑卒中模型 | 磁珠分选细胞 | β-半乳糖苷酶染色 |
| 栓塞性脑梗死模型 | 流式分选细胞 | 镀银染色 |
| 脑出血模型 | 开机费 | movat五色染色 |
| 脑损伤模型 | 单色 | 维多利亚蓝染色 |
| 脊髓损伤模型 | 双色 | 免疫组化 |
| 帕金森模型 | CBA多细胞因子流式检测 | 免疫组化预式 |
| 老年痴呆模型 | 组织/血液细胞制备 | 免疫组化正式 |
| 应激模型 | 组织单细胞制备 | 免疫荧光(石蜡-单标) |
| 骨骼疾病模型 | 中性粒细胞提取 | 免疫荧光(石蜡-双标) |
| 骨折模型 | 其他样本细胞制备(如血液等) | 免疫荧光(石蜡-三标) |
| 骨缺损模型 | 外周血PBMC分离 | 免疫荧光(冰冻-单标) |
| 风湿免疫性关节炎模型 | 线粒体组学 | 免疫荧光(冰冻-双标) |
| 骨关节炎模型 | 线粒体膜电位检测-流式法 | 制片前处理 |
| 五官疾病模型 | 线粒体膜电位检测-免疫荧光法 | 石蜡组织包埋 |
| 眼科疾病模型 | 线粒体ROS生物含量检测--流式 | 特殊包埋(细胞、材料、眼球等) |
| 鼻腔疾病模型 | 线粒体ROS生物含量检测--免疫荧光 | 软化(肝硬化、皮肤结痂、植物等) |
| 皮肤疾病模型 | 线粒体通透性转换孔(mPTP) | 骨组织脱钙(小) |
| 皮肤损伤模型 | 溶酶体免疫荧光法 | 骨组织脱钙(大) |
| 肿瘤疾病模型 | 线粒体+溶酶体共定位 | 骨组织EDTA脱钙(小) |
| 原位瘤模型 | 内质网 | 骨组织EDTA脱钙(大) |
| 转移瘤模型 | 线粒体钙瞬时变化检测-流式 | 石蜡白片 |
| 皮下植瘤模型 | ATP检测 | 细胞爬片 |
| ADP检测 | ||
| AMP检测 | ||
| 流式 | DNA/RNA半定量检测 | 基因编辑工具 |
| 组织细胞悬液处理 | pcr检测mRNA | 合成(3保1)片段/质粒/引物合成 |
| 细胞处理 | microRNA检测 | 质粒载体构建 |
| 血液标本处理 | LncRNA表达量的检测 | 过表达腺病毒载体构建包装 |
| 细胞刺激培养 | CirRNA表达量的检测 | shRNA腺病毒载体构建包装 |
| 单色检测 | 凝胶电泳 | 过表达慢病毒载体构建包装 |
| 双色检测 | 基因合成 | shRNA慢病毒载体构建包装 |
| Annexin V/PI凋亡 | <300 | 过表达腺相关病毒载体构建包装 |
| 细胞周期 | 300-1,500 | shRNA腺病毒载体构建包装 |
| 1500 - 5000 | 稳转细胞株 | |
| >5000 | ||
| 特殊序列 | ||
| ELISA | WB | qPCR |
| 组织匀浆处理 | 蛋白提取及定量一 | RNA抽提 |
| ELISA(不含试剂盒)48T/kit | WB检测一(10孔膜/指标) | mRNA引物设计及合成 |
| ELISA(不含试剂盒)96T/kit | 灰度值分析及作图一(10孔膜/指标) | miRNA引物设计及合成 |
| ELISA(含国产试剂盒)48T/kit | 蛋白提取及定量二 | LncRNA引物设计及合成 |
| ELISA(含国产试剂盒)96T/kit | WB检测二(15孔膜/指标) | CircRNA引物设计及合成 |
| 灰度值分析及作图二(15孔膜/指标) | mRNA RT-qPCR | |
| miRNA RT-qPCR | ||
| LncRNA RT-qPCR | ||
| CircRNA RT-qPCR |
上一篇:细胞辐照
下一篇:内皮细胞培养实验服务
