五分钟文献解读之《肿瘤来源的外泌体miR-934诱导巨噬细胞M2极化促进结直肠癌肝转移》
时间:2022-01-14 阅读:1951
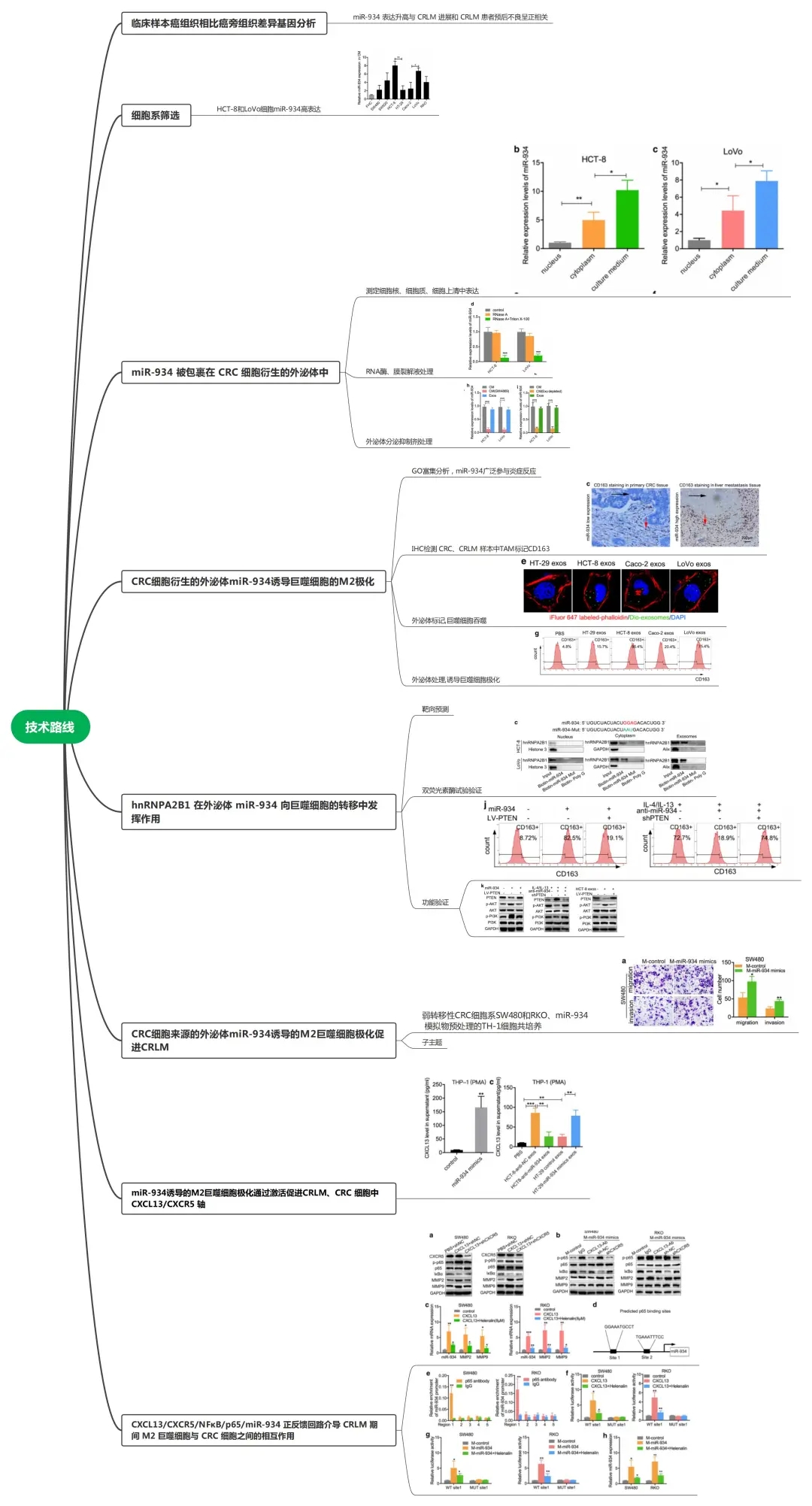
——肿瘤来源的外泌体miR-934诱导巨噬细胞M2极化促进结直肠癌肝转移 期刊:j hematol oncol 影响因子:10.743 接收:2020.11 研究背景 结直肠癌肝转移 (CRLM) 尽管手术、化疗、靶向治疗和免疫治疗相结合,部分提高了结直肠癌(CRC)治疗的临床疗效,但CRC的发病率仍位居第三,是癌症相关死亡的第二大原因。大约 50%相关死亡源于结直肠癌肝转移 (CRLM),CRLM 是最常见的继发性肝癌之一,由肿瘤细胞与肝脏中 TME 之间的相互作用介导。 技术路线 总结与思考 CRLM是最常见的继发性肝癌之一,由肿瘤细胞与肝脏中TME之间的相互作用介导。肿瘤转移前龛位是由细胞间相互作用调节的动态系统,负责肿瘤进展和远处转移。在本研究中,证明miR-934在CRLM中高度表达,并且与CRLM患者的预后不良显着相关。 同时发现富含miR-934的外泌体可以通过介导结直肠癌细胞和TAM之间的串扰并形成转移性微环境来促进CRLM。肿瘤细胞和TAMs之间外泌体miR-934调节的相互作用揭示了CRLM的分子机制,并解释了为什么所有CRC患者不会发生肝转移。 在本研究中,证明了由CRC细胞来源的外泌体miR-934诱导的巨噬细胞M2极化可以通过CXCL13 / CXCR5 / NFκB / p65正反馈回路促进CRLM,这导致肿瘤细胞和TAM之间的持续串扰,形成炎症微环境以培养CRLM。文中研究强调,CRLM的发展是一个复杂的过程,涉及由关键基因调节的多种分子相互作用。 结论 证明了 CRC 衍生的外泌体 miR-934 可以通过下调 PTEN 表达和激活 PI3K/AKT 信号通路来诱导 M2 巨噬细胞极化。 发现外泌体 miR-934诱导极化的 M2 巨噬细胞可以通过 CXCL13/CXCR5/NFκB/p65/miR-934 正反馈回路促进 CRLM。 阐明了一种促进 CRLM 的新分子机制,这是肿瘤细胞与 TAM 相互作用的基础,这将有助于开发有效的 CRLM 预防和治疗策略。 血清外泌体中 miR-934 的高表达与 CRLM 相关,这表明它可能是液体活检的有前途的生物标志物。 此外,靶向外泌体miR-934介导的肿瘤细胞和TAMs之间的串扰可能为CRLM的治疗提供新的策略。 文献涉及的实验技术 以上文献涉及的实验技术,均可在晶莱生物展开。 【晶莱生物】是一家专注于生物医学领域内科研学术服务的高新技术企业,致力于打造国内一流的生物技术服务品牌。为生物医学研究者提供动物造模、细胞生物学、基因组学、蛋白鉴定及分析、病理组化、表观遗传学等多个实验平台服务。