没有外界输入,前脑类器官也能“长出”神经网络?
时间:2026-04-07 阅读:102
【全篇阅读大约 6 分钟,文末附原文下载链接】
写在前面
这篇发表于《Stem Cell Reports》的研究,回答了在脑类器官研究里一个很难回避的问题:在缺乏感觉输入和长程连接的条件下,前脑类器官能否依靠自身发育程序,自发形成具有一定拓扑特征的神经网络?
文章显示,背侧前脑类器官和腹侧前脑类器官虽然都能形成网络,但最终呈现出的组织方式并不相同。其真正推进的,不只是脑类器官构建本身,而是“细胞组成如何塑造网络结构”这一层面的理解。
做脑类器官研究的人,几乎都会碰到同一个问题:培养皿里那团神经元,究竟只是“活着”,还是已经开始彼此连接,慢慢长成一个真正有组织的网络?
这篇《Stem Cell Reports》抓住的,正是这个问题。
它不再停留在“前脑类器官有没有长出来”这一步,而是继续往前追问:在没有感觉输入、没有真实脑区长程连接、也缺乏完整体内微环境的前提下,前脑类器官能不能仅凭自身的发育程序,逐步组织出具有一定拓扑特征的神经网络?
文章给出的答案是肯定的。
更值得注意的是,背侧前脑类器官和腹侧前脑类器官虽然都能形成网络,但它们最后长出来的,并不是同一种网络。也就是说,这篇文章真正往前推的,是“不同类型的细胞会把网络带向什么方向”这个问题。
在讨论网络之前,研究者先把模型本身做稳了。因为只有区域身份清楚、细胞组成稳定,后面的网络分析才有解释意义。
这一步的重要性在于,如果区域身份不清、细胞组成不稳,那么后面看到的任何“网络现象”,其实都很难被真正解释。
从前面的表征结果来看,背侧前脑类器官在早期已经出现 Sox2、Pkcζ、N-cadherin 等神经上皮和极性相关标志;
随着培养推进,又逐步出现 Tbr1、Brn2、Ctip2、Map2、GABA,以及少量 Pvalb⁺ 和 Sst⁺ 细胞。
单细胞测序进一步提示,这套体系不仅具备前脑相关细胞谱系特征,而且在不同小鼠胚胎干细胞系之间具有较好的可重复性。
换句话说,这篇文章先处理的是模型可靠性,而不是直接进入功能层面的讨论。
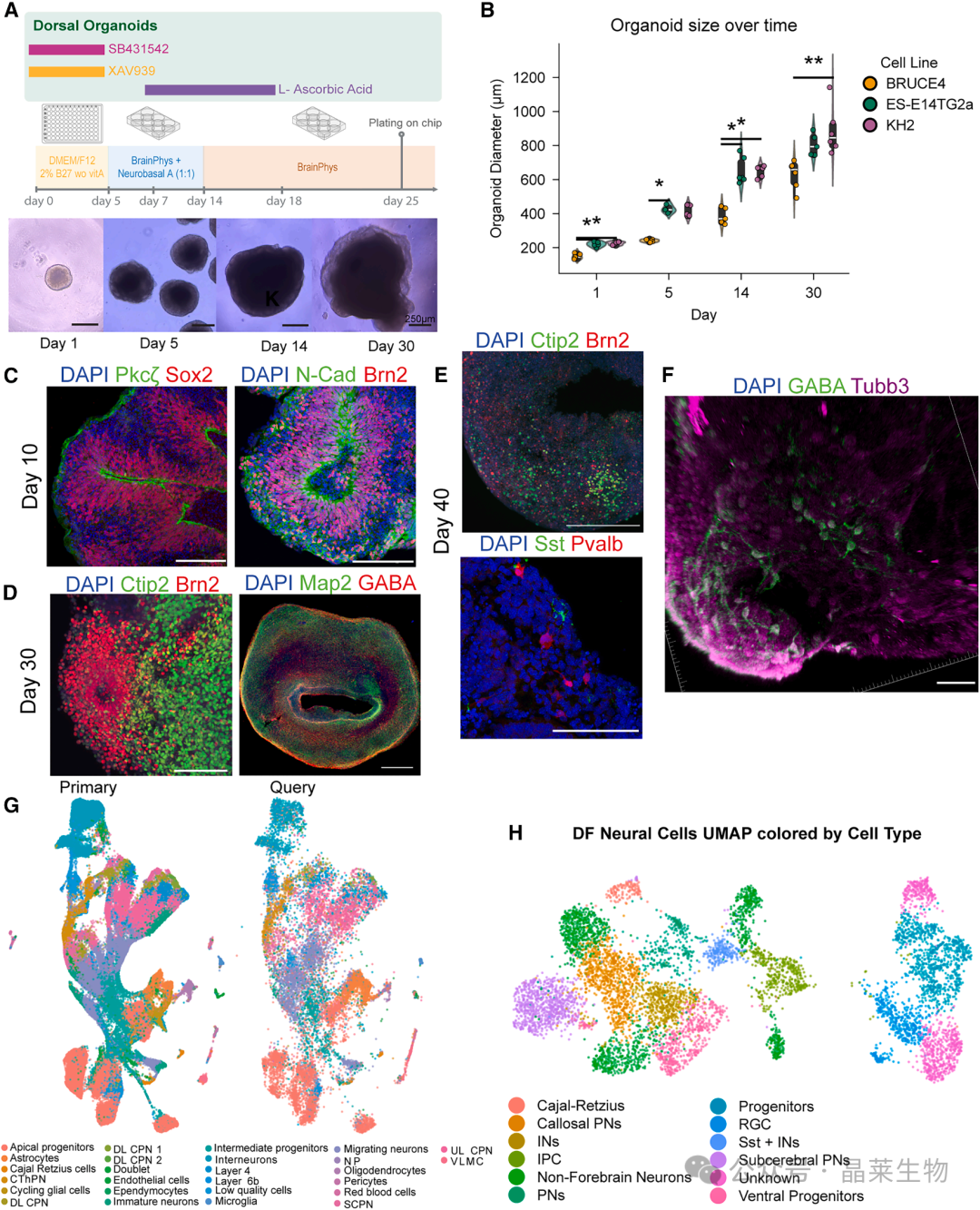
背侧前脑类器官构建与早期表征
在模型已经具备明确前脑身份的基础上,研究者进一步引入高密度多电极阵列,连续追踪不同发育阶段的神经活动。
这里真正想回答的,不是类器官里“有没有电活动”,而是这些神经元之间是否在逐步建立协同关系。
结果显示,随着培养时间延长,背侧前脑类器官的整体放电频率持续升高;与此同时,用来衡量神经元时间相关性的 STTC 也同步增加。
这意味着类器官中的神经元,并不是彼此孤立地发放,而是在逐步形成更加协调、更加有组织的活动模式。更重要的是,这里的信号已经不只是单个神经元在发放,而是神经元之间开始出现可追踪的网络联系。
文章也同步指出,这种同步性是一路增强的,并没有完全重现体内皮层发育中更复杂的成熟轨迹。这也提示我们,类器官虽然已经具备自发成网的能力,但距离真实脑发育仍然存在明显差距。
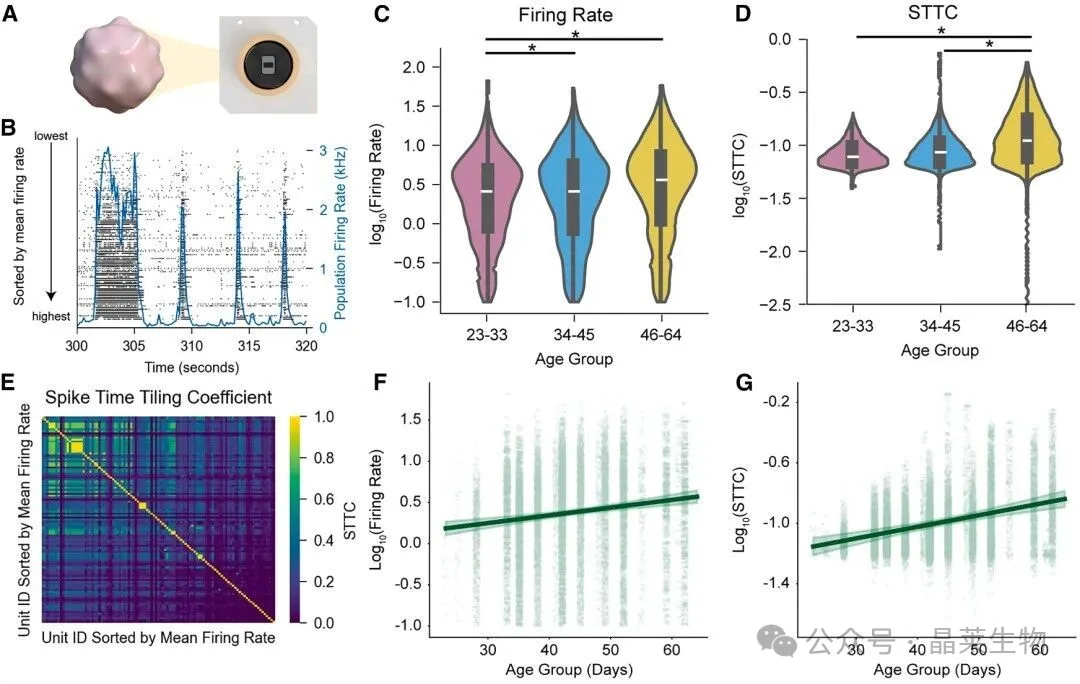
背侧前脑类器官的电生理发育轨迹
基于前面观察到的同步增强现象,进一步把问题落到了兴奋—抑制平衡上。
因为网络变得更同步,既可能来自兴奋性驱动增强,也可能与抑制性回路调控有关。
为明确这一点,文章设计了药理学干预实验。
结果表明,阻断 AMPA/Kainate 受体后,网络爆发活动明显受损,STTC 也显著下降;阻断 NMDA 受体后,连接性变化相对有限;而当 GABA_A 受体被阻断后,平均放电频率变化并不明显,但网络同步性却显著上升。
它说明抑制性回路的作用,并不只是简单压低总体活动水平,更重要的是限制网络无差别同步,帮助系统保留层次和边界。
换句话说,抑制性神经元不是网络里的“配角”,而是在塑造网络最终会长成什么样。
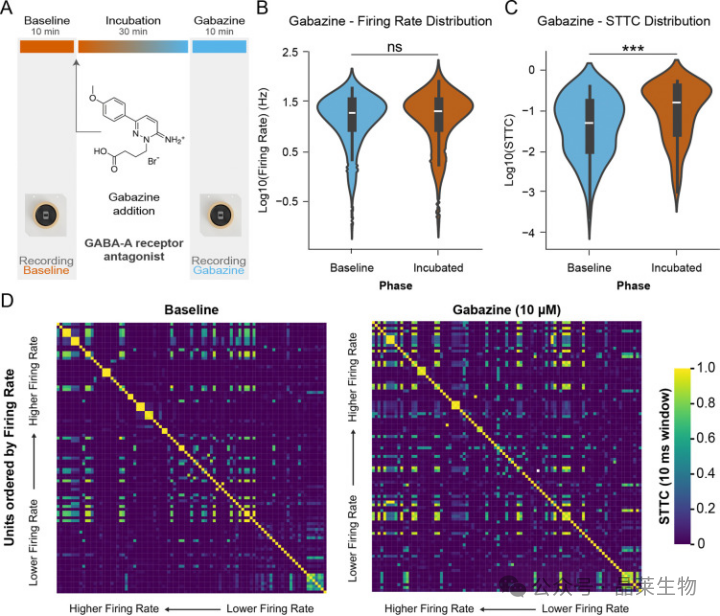
兴奋—抑制平衡对背侧前脑网络同步的影响
基于抑制性回路可能是网络分化的关键变量,文章进一步建立了腹侧前脑类器官模型。
这样做的目的,是把抑制性中间神经元富集的系统单独拉出来,从而更直接地比较细胞组成与网络特征之间的关系。
从结果来看,腹侧前脑类器官的区域身份是清楚的。
Pax6 在背侧模型中更高,而 Nkx2.1 在腹侧模型中明显富集;后续的免疫染色和分子结果也支持腹侧模型具备更强的抑制性中间神经元特征,包括 GABA、Sst、Pvalb、WFA 以及 Cox6a2 等信号。
也就是说,这篇文章后面比较的并不是两个“长得不太一样的类器官”,而是一组具有明确生物学对照意义的系统:一个更偏兴奋性投射神经元,一个更偏抑制性中间神经元。
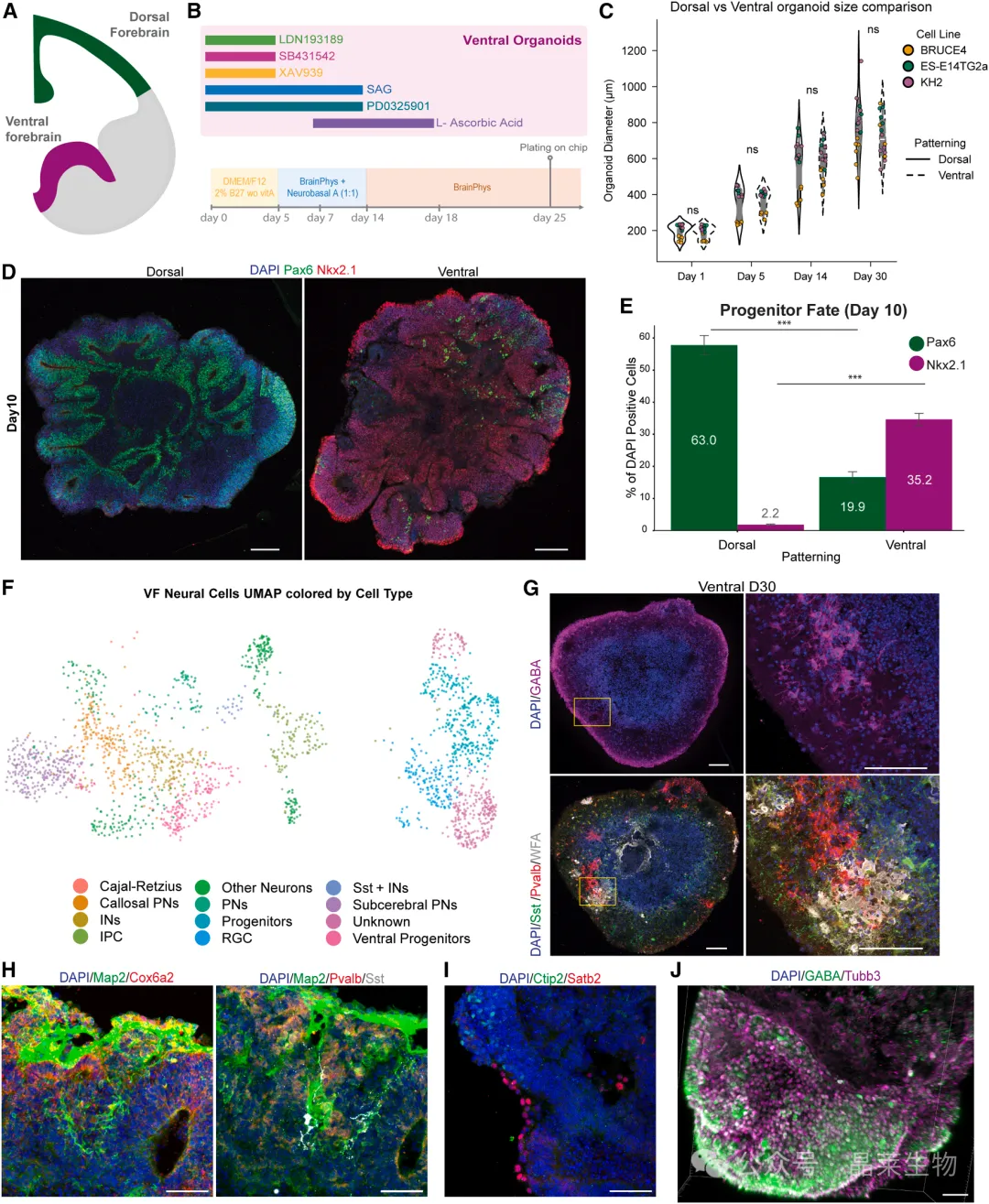
腹侧前脑类器官的建立与细胞组成特征
在两套模型已经具备可比性的基础上,文章进一步对腹侧前脑类器官进行了与背侧模型相同的电生理追踪。
这里有一个特别值得强调的点:如果只看放电频率,两者并没有完全相反的趋势。腹侧前脑类器官同样会随着发育变得活跃。因此,这里的差异从来不是“能不能放电”。
真正拉开距离的是同步性的演化方向。背侧前脑类器官的 STTC 会随着发育持续升高,而腹侧前脑类器官则保持得更加平稳,没有继续朝着“全网同步不断增强”的方向推进。
这说明,腹侧前脑类器官并不是没有形成网络,而是形成了另一种组织方式不同的网络。
抑制性中间神经元的加入,并没有简单削弱活动,而是在改变网络的收敛路径,使系统从整体同步转向更具层次感的局部组织。
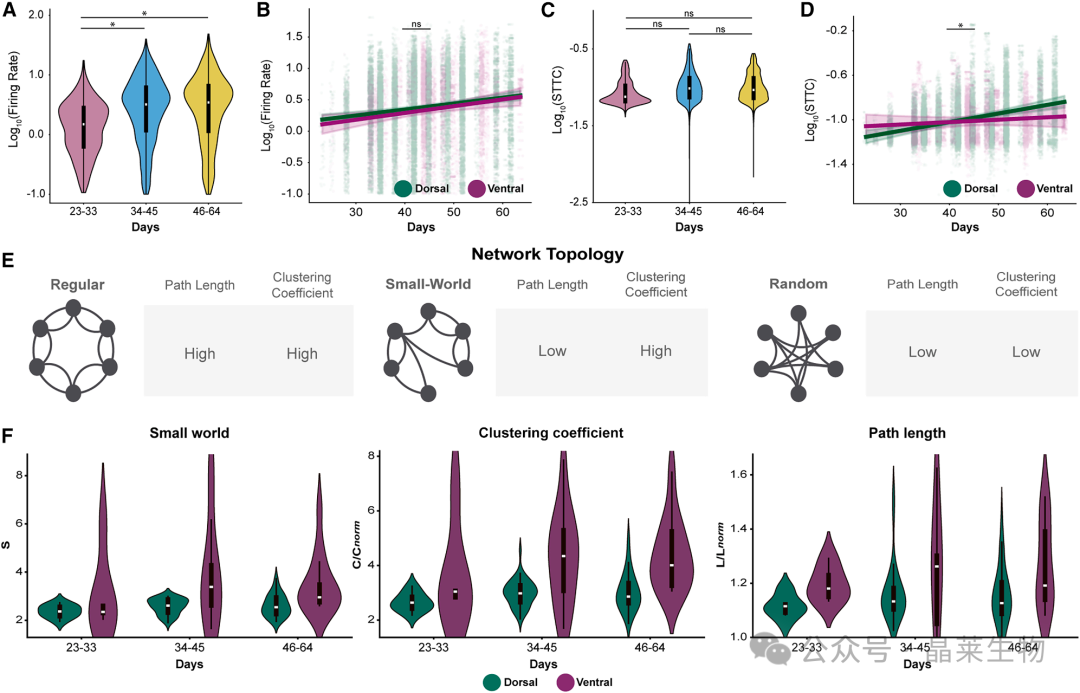
背侧与腹侧前脑类器官呈现不同的神经动态轨迹
在同步模式已经出现分化之后,文章进一步把分析推进到网络拓扑层面,关注这些神经元究竟是以怎样的方式被组织起来。
结果显示,两类类器官都形成了明显的小世界网络,这说明类器官体系本身已经具备自发建立脑网络经典拓扑特征的能力。
进一步比较发现,腹侧前脑类器官的小世界指数整体更高,而这一优势主要来自更强的局部聚类,而不是更短的路径长度。
从网络组织方式来看,背侧前脑类器官更接近整合性增强的主干网络,而腹侧前脑类器官则更接近局部连接紧密的模块化结构。
前者更强调整体协同,后者更强调局部回路。
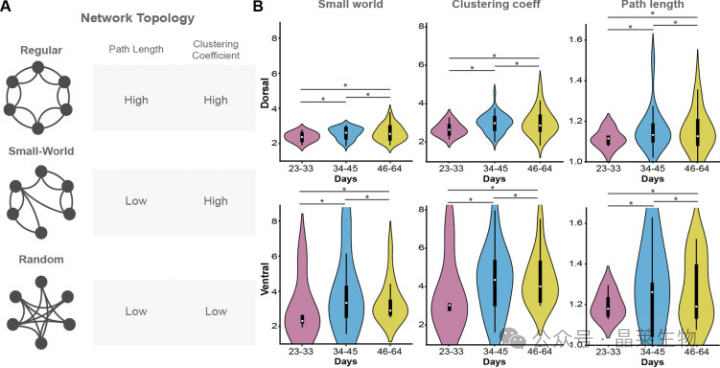
背侧与腹侧前脑类器官的小世界网络与聚类特征
在后续分析中,文章进一步比较了核心—边缘结构、hub分布以及功能社区差异。
结果显示,背侧前脑类器官在发育中后期更强调核心区与外围之间的整合,而腹侧前脑类器官则更容易形成相对独立的局部模块。与此同时,背侧模型中的高 hub 节点分布更广,更像是在支撑整张网络;腹侧模型中的高 hub 节点则更倾向于聚集成局部簇。
到了功能层面,这种差异表现得更加直观。
成熟阶段的背侧前脑类器官,更容易稳定地招募一批反复参与活动的“骨干节点”;腹侧前脑类器官的模块招募时间则更分散,整体上呈现出更高的灵活性和异质性。
综合来看,背侧前脑类器官更像一个主干更清晰、整合度更高的网络;腹侧前脑类器官则更像一个边界更明确、局部模块更活跃的系统。
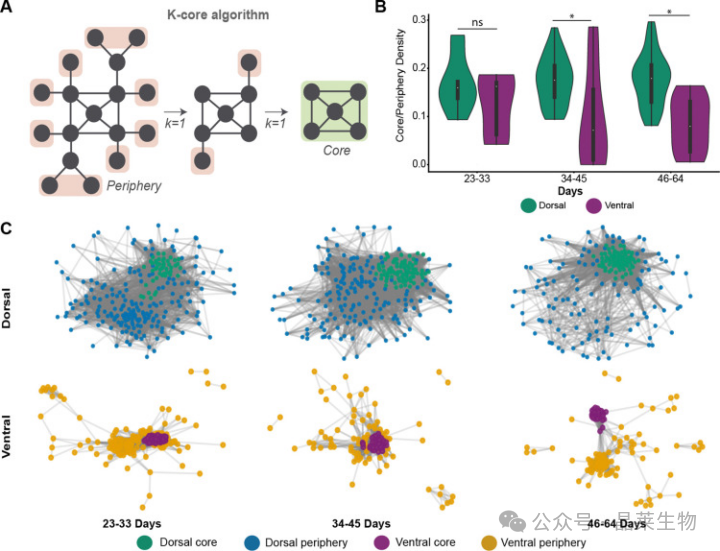
背侧与腹侧前脑类器官的核心—边缘结构差异
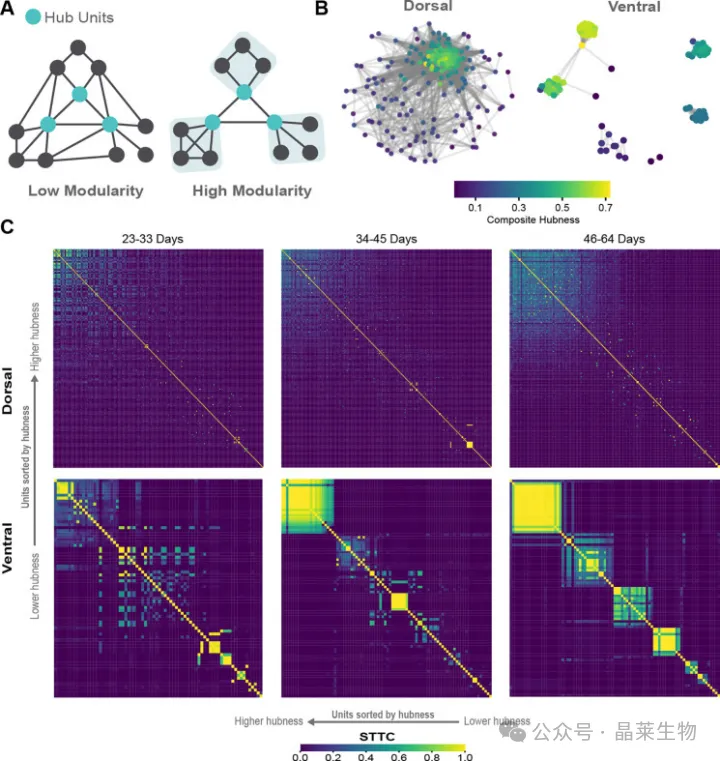
背侧与腹侧前脑类器官的 hub 组织与模块化差异
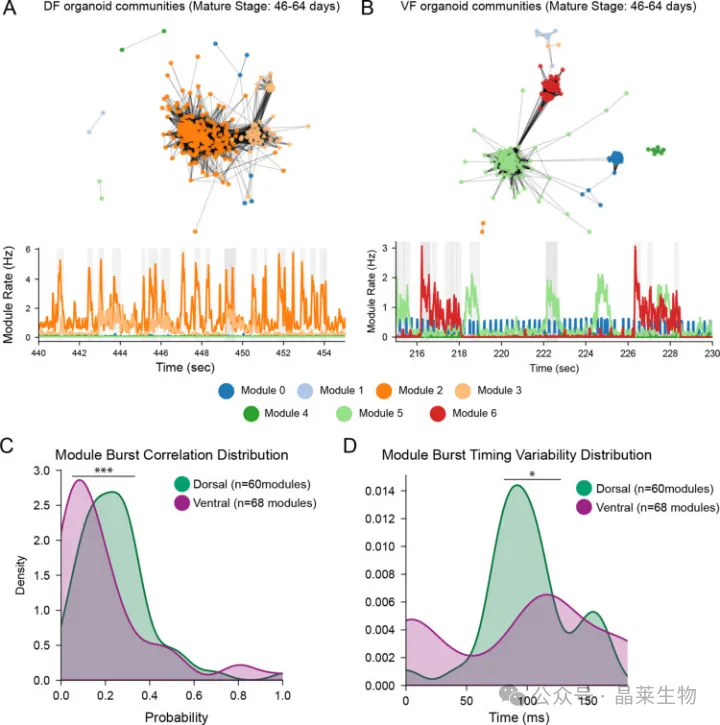
背侧与腹侧前脑类器官的功能社区与 burst 结构差异
过去很多脑类器官工作更常回答“分化得对不对”“marker 是否齐全”这类问题,而这篇文章开始认真讨论:一个类器官里的神经元,是否已经足以搭起具有层次感的网络。
细胞组成并不是一个静态背景变量,而是决定网络命运的重要因素。尤其是抑制性中间神经元,并不是后期用于“修补系统”的补充角色,而是能够从根本上改变网络如何同步、如何分区,以及如何建立功能模块。

(扫描二维码可下载原文)
如果把这篇文章放回到类器官平台建设的语境里,它传递出的信号非常明确:未来研究者需要的,不会只是一个“能养出来的模型”,而是一个能够稳定构建、清楚表征、具备功能 readout,并且可以继续承接机制研究和药效评价的系统。
这也是为什么,我们一直更看重类器官平台从“模型构建”走向“功能建模”的能力升级。对于脑类器官、疾病模型、药物筛选和机制研究来说,真正有价值的,不是某一个孤立模型,而是一条从模型建立、分子验证到功能检测和数据解析能够连续打通的技术链。
这篇文章是一个很清晰的行业信号:未来真正有竞争力的类器官平台,不只是把模型做出来,更要把模型“读明白”。
关于晶莱















