【五分钟讲实验】胶质母细胞瘤(GBM)模型细胞系选择及动物模型构建方法
时间:2023-12-25 阅读:1335胶质母细胞瘤是最常见的恶性原发性中枢神经系统肿瘤,也是最使人衰弱的癌症之一。胶质母细胞瘤(GBM)是最常遇到的恶性原发性中枢神经系统(CNS)肿瘤,占所有恶性原发性中枢神经系统肿瘤的50.1%和原发性中枢神经系统肿瘤的14.2%。胶质母细胞瘤的年发病率约为35/100万,男女比例为1.6:1。该发病率随年龄增长而增加,在≥65岁年龄组中约为130/100万。
本文提供了现有模型的整体和全面图景,详细说明了每种模型的优点和缺点,利用它们进行胶质母细胞瘤研究的适当方法,以及推进它们的潜在途径。
目前还有3D 体外建模和微流控的新兴领域,这些领域增强了体外 GBM 研究的能力,并为未来具有成本效益和节省时间的研究提供了有前途的方法。
GBM研究中使用的细胞系
不同神经胶质瘤细胞系的遗传和组织病理学特征
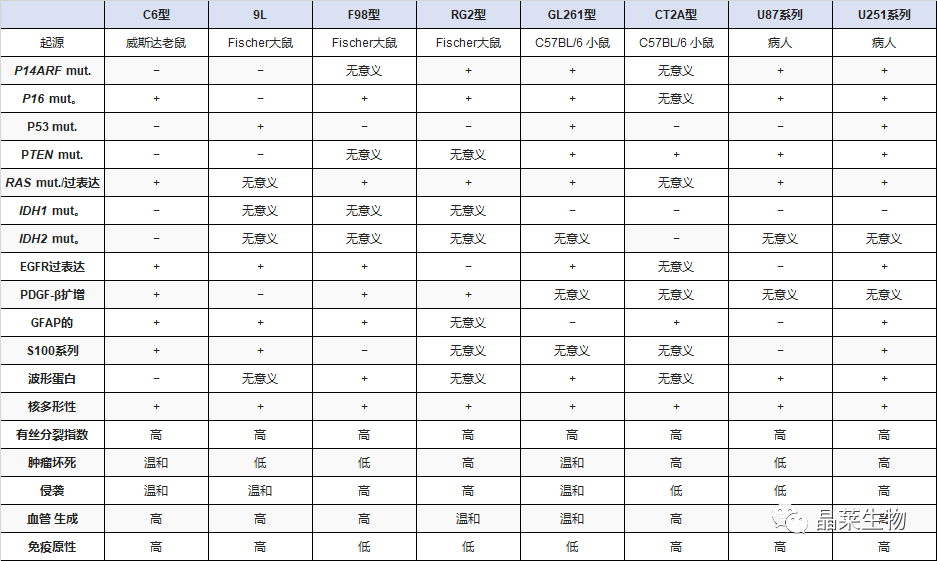
1. C6细胞系
C6 细胞系是 GBM 研究中最受欢迎的细胞系之一。它使用暴露于近交Wistar大鼠的N-甲基亚硝基脲星形胶质细胞8个月而开发。这些细胞具有野生型 Tp53 基因。
亚硝基脲诱导的大鼠神经胶质细胞通常纯合地失去其p16/Cdkn2a/Ink4a基因位点。血小板衍生生长因子 (PDGF)-β、表皮生长因子受体 (EGFR)、胰岛素样生长因子 (IGF)-1、Erb3/Her3 前体蛋白和 Rb 基因表达增加。TGFα前体(而非TGFα基因本身)过表达,这些特征与人神经胶质瘤细胞相似。成纤维细胞生长因子9(fibroblast growth factor 9, FGF-9)和FGF-10的表达降低。此外,Ras活性的增加与在人神经胶质瘤细胞中观察到的相似。与人神经胶质瘤不同,IGF-2的表达降低。该细胞系的另一个缺点是C6细胞系中不存在IDH-1和IDH-2突变。缺乏 IDH-1 和 -2 突变会降低 C6 细胞对化疗的敏感性。然而,有研究报道,可以引入IDH2的人工突变,它挽救了细胞迁移的特性,使细胞对化疗更敏感。与人GBM不同,C6细胞系为GFAP阳性。
该系的主要缺点是触发同种异体免疫应答。因此,C6系列在Wistar和BDX大鼠的免疫治疗研究中的效用有限。
2. 9L细胞系
通过向Fischer大鼠静脉注射5mg/kgN-甲基亚硝基脲26周来开发9L细胞系。当9L细胞在大鼠脑内植入时,它们具有肉瘤组织学。因此,9L衍生的肿瘤模型也称为胶质肉瘤。
TGFα 和 EGFR 过表达。FGF-2、FGF-9、FGFR-1和PDGF-β的表达降低。该肿瘤模型具有高免疫原性,降低了其在免疫治疗研究中的效用。该模型具有突变的Tp53基因。
对具有9L细胞的大鼠肿瘤模型的检查显示CD8+ T淋巴细胞浸润是抗肿瘤免疫反应的证据。
3. F98细胞系
该细胞系PDGF-β、Rb、Ras、EGFR、细胞周期蛋白D1和细胞周期蛋白D2表达增加,波形蛋白和GFAP染色阳性。F98衍生的肿瘤免疫原性较弱,CD3+ T细胞浸润不显著,这一特性使其可用于免疫治疗研究。
该系的乳腺癌1(BRCA1)基因表达降低,导致DNA修复中断,对某些化疗药物(铂和紫杉醇治疗)和光子疗法的反应降低。F98细胞对BNCT和6兆伏(MV)放疗(卡铂或顺铂联合颅内给药)显示出良好的反应。4. RG2细胞系
该细胞系是在妊娠第20天通过静脉注射50mg/kg N-乙基亚硝基脲对怀孕的Fischer大鼠产生的。由于相似的生成过程,它与 F98 细胞系有一些相似之处。
RG2细胞表现出非常侵入性的模式,这使其成为GBM的合适模型。
RG2 细胞系的 PDGF-β、IGF-1、Erb3/Her3 前体蛋白、Ras 和 D2 的表达增加。它们具有野生型Tp53基因和p16/Cdkn2a/Ink4基因位点的表达缺失。5. GL261细胞系
GL261细胞系是通过颅内注射3-甲基胆兰素到C57BL/6小鼠体内开发的。
该细胞系存在p14、p16、磷酸酶和张力蛋白同源物(PTEN)、K-ras和EGFR突变。GFAP阴性,波形蛋白阳性。H-ras表达降低。GL261细胞具有可检测到的MHC I类表达水平,这使得它们对自然杀伤细胞具有中等敏感性。可通过IFN-γ刺激而增加,检测到MHC II.类的表达。
在组织学水平上,GL261诱导的肿瘤模型显示假性栅栏坏死、血管周围增生和核多形性。GL261肿瘤也显示出与室管膜母细胞瘤的组织学相似性。
举例:使用植入GL261细胞的胶质母细胞瘤小鼠模型,免疫检查点抑制剂抗程序性死亡-1(抗PD1)被证明与谷氨酸调节因子BHV-4157具有协同作用。
6. CT2A细胞系
CT-2A细胞系是在C57BL/6小鼠中通过甲基胆蒽诱导开发的。该细胞模型显示有丝分裂指数高、细胞密度增加、细胞核多态性、出血区、假性栅栏坏死(中央坏死区)、高血管生成和微血管浸润。
对周围实质的侵袭性较弱,该细胞系在体内生长时显示出尖锐的肿瘤边界,这与人类GBM不同。然而,与其他胶质瘤细胞系相比,该细胞系在体外显示出更高的侵袭性和迁移性。该细胞系具有野生型p53和IDH1,缺乏PTEN表达。GFAP染色呈阳性,常见于肿瘤边缘区域和肿瘤内小血管壁附近。
7. U87细胞系
该系存在p14、p16和PTEN基因突变。U87细胞系不表达S100和GFAP,尽管它来源于神经胶质来源。波形蛋白呈阳性。表现为血管形成较弱。
U87细胞无VEGFR-1表达,VEGFR-2表达低,VEGF水平升高。IDH1为野生型。CD31、VE-cadherin、Tie1或Tie2作为内皮细胞特异性标志物未表达。然而,这些细胞的CD133标志物染色呈阳性,这允许神经球的形成。体外显示出较高的菌落形成和迁移潜力。
8. U251细胞系
U251细胞系来源于人GBM,是最常用的患者来源细胞系之一。
该系含有 p14、p16、PTEN 和 EGFR 基因突变; 它还显示PI3K上调和U251肿瘤中的无功能突变Tp53基因。该细胞系的S100、GFAP和波形蛋白呈阳性。它显示出快速的生长模式。U251衍生的肿瘤模型Ki-67染色率高(>50%),坏死周区域对缺氧诱导因子-1-α(HIF1-α)和Caspase-3染色呈阳性。肿瘤的CD133也呈阳性。
不同神经胶质瘤细胞系的研究用途
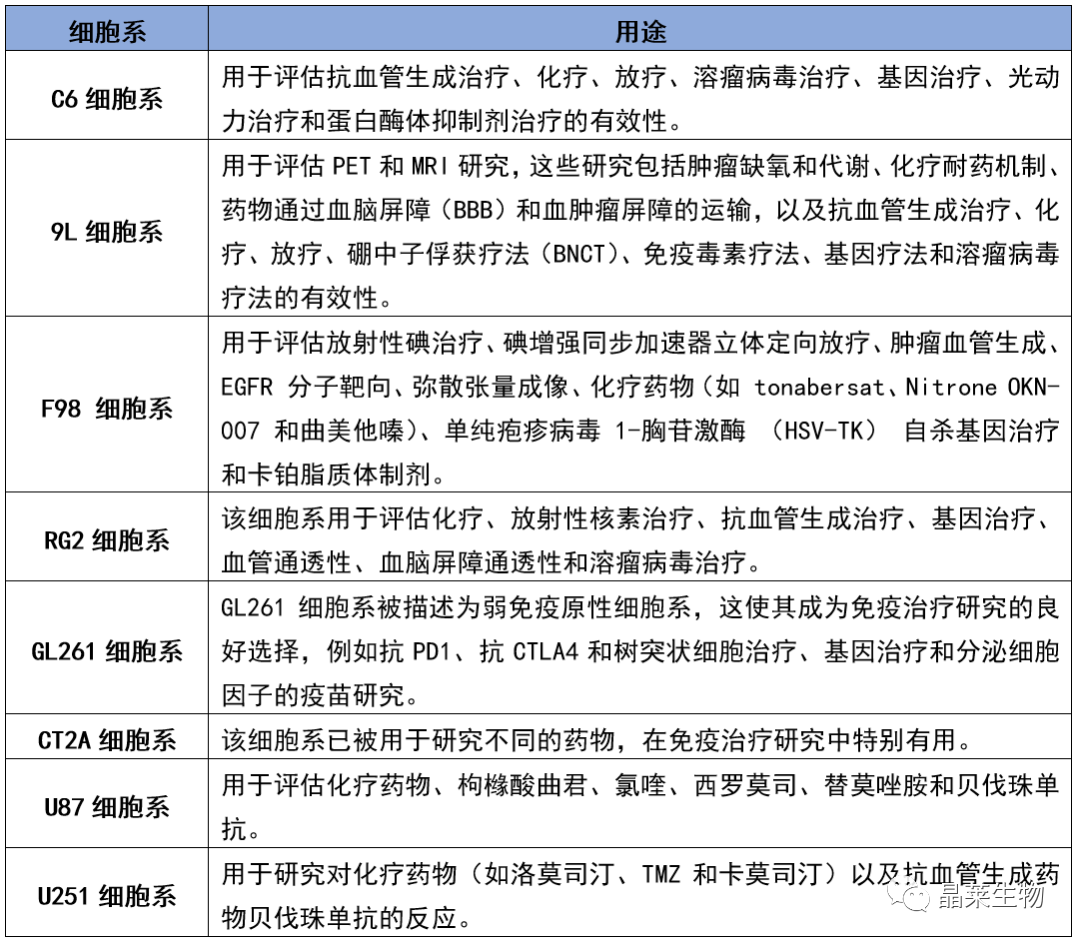
GBM动物模型
1. 用于生成GBM动物模型的不同方法
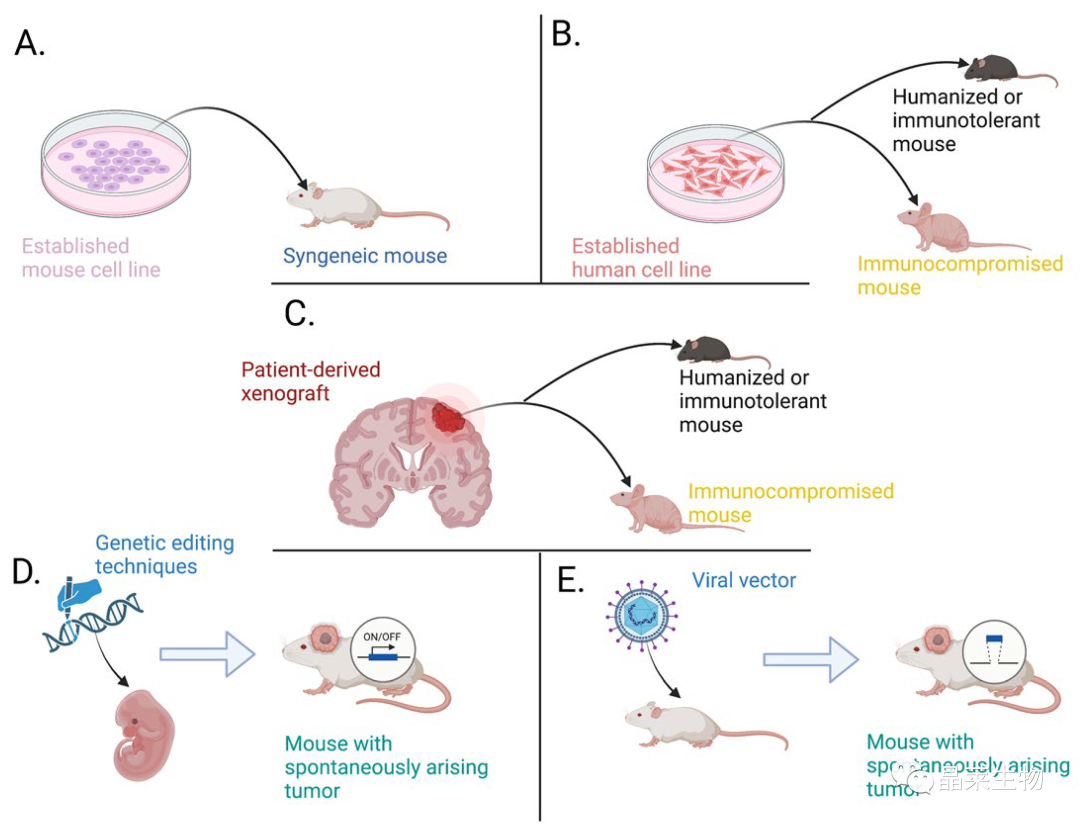
(A) 将已建立的细胞系植入同一物种的同源动物中,允许使用免疫功能正常的宿主。
(B) 使用最初从患者肿瘤样本中获得并在培养物中繁殖的已建立的人类细胞系需要植入免疫功能低下、人源化或免疫耐受的动物模型中。
(C) 使用患者来源的异种移植物涉及将患者组织植入免疫功能低下或人源化/免疫耐受的宿主中;然而,这种类型的异种移植不包括体外传代作为中间步骤。
(D)动物胚胎的基因工程或基因工程亲本的育种可以产生动物模型,这些动物模型可以以可以在时间和空间上控制的方式自行发展肿瘤。
(E)以类似的方式,使用病毒载体转染动物允许以时间和空间控制的方式“从头开始”产生肿瘤。
2. 举例:免疫耐受小鼠模型
通过使用阿巴西普(一种免疫球蛋白,通过与 CD80/86 结合并阻止随后的 T 细胞活化来模拟 CTLA-4 的作用)和 MR1(一种抗 CD154 抗体,可阻止 T 细胞上的 CD154 与抗原呈递细胞上的 CD40 之间的刺激相互作用)的 T 细胞药物治疗阻断来实现的。在移植人GBM细胞后第0、2、4和6天,将这些药物腹膜内输送至免疫功能正常的C57BL6。由此产生的模型成功地培养了颅内肿瘤,并保留了与宿主免疫系统的相互作用,这密切概括了人类GBM的病理生理发展和特征。
3. 不同实验动物应用对比
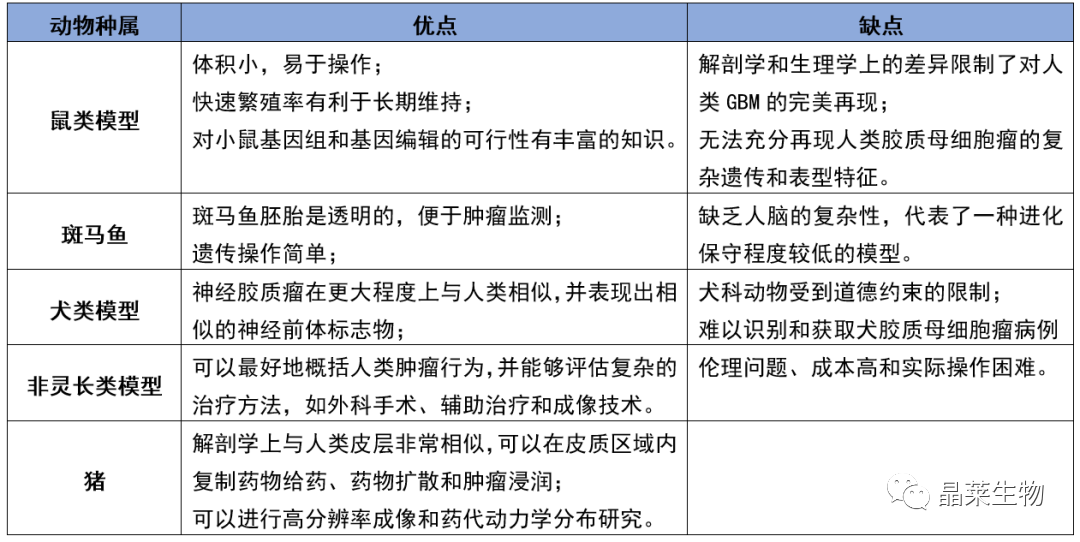
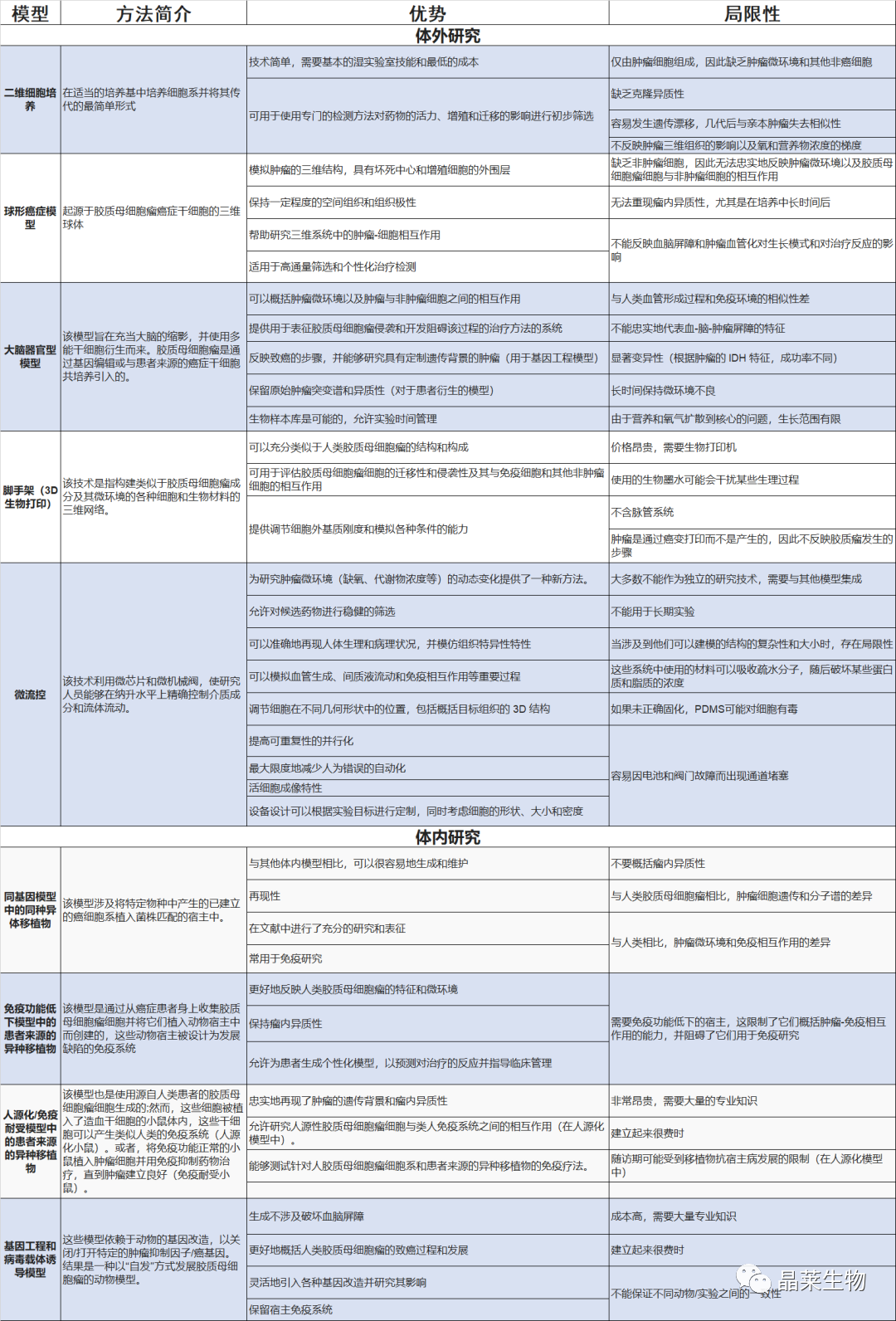
胶质母细胞瘤研究的体外和体内模型总结
关于晶莱
关注公众号,了解更多!