【备战2019国自然之干细胞研究】频频中标的原因竟然是......
时间:2018-11-08 阅读:2677干细胞研究热点持续上升
这些年,干细胞研究热点持续上升,从科学核心网(Web of Science Core Collection)上统计的文章数量可见一斑(图1)。正是由于干细胞研究热度的持续上升,使得相关领域的研究得到资助的机率也大为提高。据统计,2018国自然资助项目中,干细胞领域共496项中标,我们推测2019年国自然依然会对干细胞研究保持高资助态势。
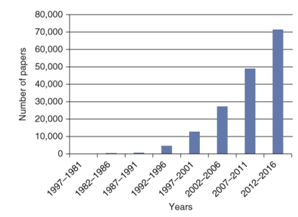
图1. WOSCC上干细胞相关文章统计.
from Slack JMW. Wiley Interdiscip Rev DevBiol. (2018)
干细胞的主要特性是具有自我更新和分化潜能,天然存在的干细胞按分化潜能大小主要有两类,一类是多能干细胞,包括胚胎干细胞(ESCs, embryonic stem cells)和诱导多能干细胞(iPSCs,induced pluripotent stem cells),另一类是组织特异性干细胞,也叫成体干细胞或组织间充质干细胞(MSCs, mesenchymal stem cells)。
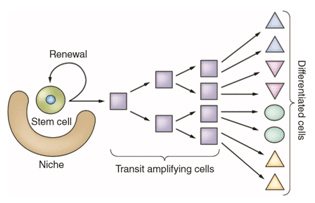
图2. 干细胞生存环境、自我更新和分化潜能.
from Slack JMW. Wiley Interdiscip Rev DevBiol. (2018)
干细胞通过一系列分子机制维持自我更新和抑制分化,这些分子标准物包括核心转录因子如OCT4,SOX2,NANOG,KLF4、端粒酶、细胞膜表面糖基化蛋白如CD34、LGR5等。但并不是说所有干细胞都具有一样的分子标志,不同来源的干细胞会有所不同。当前,干细胞研究最热两大类型:间充质干细胞和肿瘤干细胞。
间充质干细胞是多潜能非造血成体干细胞,通常表达CD90,CD105和CD73表面标志物,但不表达CD14,CD34和CD45。MSCs最初由Friedenstein于1960s年代在研究骨髓中发现,至今,MSCs可从脂肪、牙髓、胎盘、肝、肾、胰等许多其他组织中提取获得。
MSCs具有包括分化潜能、克隆形成和自我更新等独特特性,可向成骨细胞、软骨细胞、脂肪细胞、内皮细胞、肝细胞、神经细胞等定向分化,另外,MSCs还通过分泌营养因子、细胞因子等旁分泌途径对周围细胞产生影响。
正是由于其分化潜能和旁分泌特点,MSCs在组织修复和再生医学领域具有广阔应用前景而备受关注。在ClincalTrial网站以Mesenchymal stem cell为关键词就有705个临床项目在开展,其中绝大部分与组织修复和再生医学相关。
值得一提的是,近几年来,MSCs胞外微球/外泌体相关基础研究和应用研究得到了广泛关注,吸引了越来越多研究者的兴趣。干细胞通过外泌体的机制研究一般还要归结到携带的蛋白质、miRNA、lncRNA、circRNA等角度去阐述,而干细胞+外泌体+lncRNA是一个比较推荐的新型研究方向。
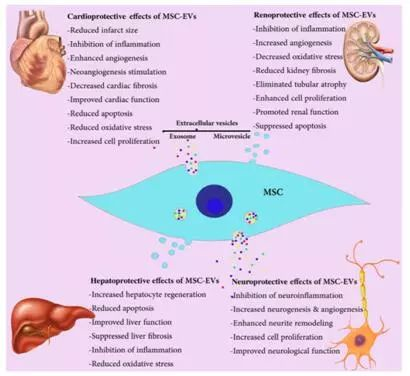
图3. MSCs来源胞外微球/外泌体在心血管、肾脏、肝脏和神经系统疾病中的治疗效应.
from Keshtkar et al. Stem Cell Research& Therapy (2018)
癌症是世界上最严重的疾病,肿瘤干细胞(CSCs, cancer stem cells)在肿瘤发生、迁徙转移、药物耐受和复发中均扮演重要角色。肿瘤干细胞具有自我更新、分化和引发新肿瘤的能力。
CSCs的自我更新能力由各种调节因子精细调节,包括Wnt/β-catenin,Notch和Hedgehog信号通路,转录因子、染色质重构复合物、非编码RNA等。此外,CSCs龛(CSCs niches)也参与CSCs自我更新的维持,从而保护CSCs免受化疗、放疗和其他内源性损伤。而且,CSCs本身能通过旁分泌途径重构其微环境,促进肿瘤的发生。
CSCs与其微环境的互作在调节CSCs自我更新和肿瘤起始中发挥重要作用。从CSCs分子标志物挖掘、CSCs与微环境的互作等方面研究CSCs在肿瘤发生、转移、药物耐受、复发等方面的研究将持续受关注。
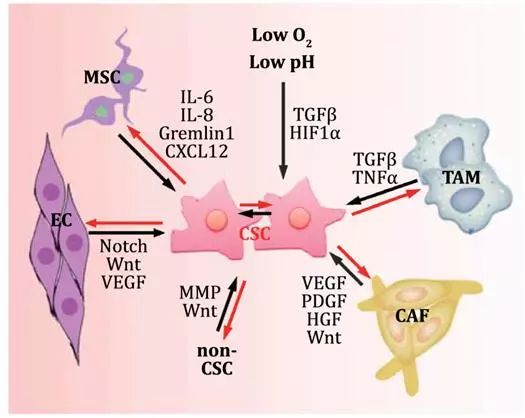
图4. CSCs与微环境的互作.
CSC: cancer stem cell,
TAM: tumor-associatedmacrophage,
CAF: cancer associated fibroblast,
MSC: mesenchymal stem cells,
EC:endothelial cells. from Zhu P and Fan Z.Biophys Rep.(2018)
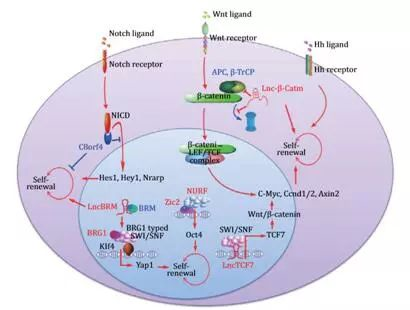
图5. 肝癌肿瘤干细胞自我更新调节因子.
红色标注为正调控因子,蓝色标注为负调控因子.from Zhu P and Fan Z. Biophys Rep.(2018)
1. Keshtkar S, Azarpira N, Ghahremani MH. Mesenchymal stem cell-derivedextracellular vesicles: novel frontiers in regenerative medicine. Stem Cell Res Ther. 2018;9(1):63.
2. Desai A, Yan Y, Gerson SL. Concise Reviews: Cancer Stem Cell TargetedTherapies: Toward Clinical Success. StemCells Transl Med. 2018.
3. Zhu P, Fan Z. Cancer stem cells and tumorigenesis. Biophys Rep.2018;4(4):178-188.
4. De Los Angeles A, et al. Hallmarks of pluripotency. Nature. 2015;525(7570):469-78.
5. Slack JMW. What is a stem cell? WileyInterdiscip Rev Dev Biol. 2018













