【五分钟讲实验】细胞衰老研究该如何入手?一文了解细胞衰老研究思路和机制
时间:2024-04-22 阅读:112细胞衰老是一个复杂的过程,涉及多种机制和调节剂。自1961年首次在体外描述以来,细胞衰老已成为生物技术公司及研究者关注的焦点,因为它与各种人类状况有关,特别是与年龄相关的疾病。研究者对细胞衰老的研究热度也愈加升高。
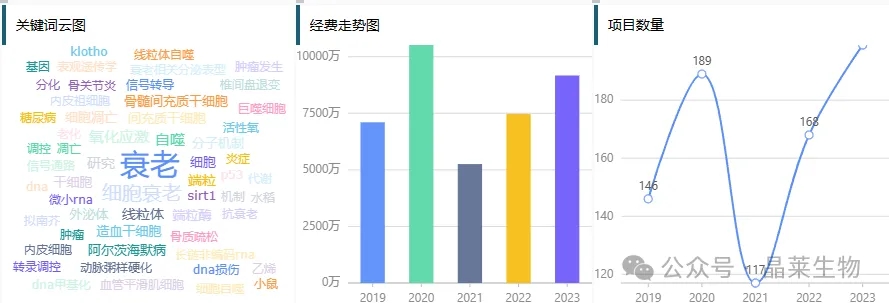
在近3年国自然的中标项目中细胞衰老项目数量每年都有增长,说明国家对细胞衰老研究的重视程度也逐年加强。
1. 细胞衰老的触发因素
细胞衰老可以由多种因素引发,包括DNA损伤、端粒功能障碍、癌基因激活和细胞器应激。这些因素都可能导致细胞进入衰老过程。
2. 细胞衰老与机体衰老的关系
海弗利克和穆尔黑德1961年的研究表明,正常培养的人类成纤维细胞在经历有限的增殖能力后,会进入不可逆的生长停滞,这被称为复制性衰老。这引发了一个假设,即组织的衰老可能是由于细胞逐渐失去增殖能力导致的。然而,这个假设花了数十年的时间才被证实。
2. 识别衰老细胞的工具
在活组织中识别并选择性地标记衰老细胞是一个关键障碍。衰老相关-β-半乳糖苷酶(SA-β-gal)活性是一个重要的生物标志物,可以帮助人们识别和检测具有衰老特征的细胞。
3. 细胞周期抑制蛋白与衰老
衰老细胞的一个显著特征是细胞周期抑制蛋白的表达增加,这些蛋白统称为周期蛋白依赖性激酶抑制剂。在这些蛋白中,p16INK4A(简称p16)在衰老细胞积累中发挥了最重要的作用,因为它对于维持持久的增殖停滞状态至关重要。
4. 细胞衰老与癌症的关系
研究发现,细胞衰老可以由过度的致癌信号或肿瘤抑制功能的丧失而过早诱导。此外,细胞衰老也可以由DNA复制异常和DNA损伤积累引起,这有助于限制受损癌前细胞的增殖。
5. 定义衰老状态的重要性
虽然衰老细胞具有一些共同特征,但并非所有衰老细胞都会表现出这些特征。因此,同时测试多种生物标志物来定义衰老状态是非常重要的。
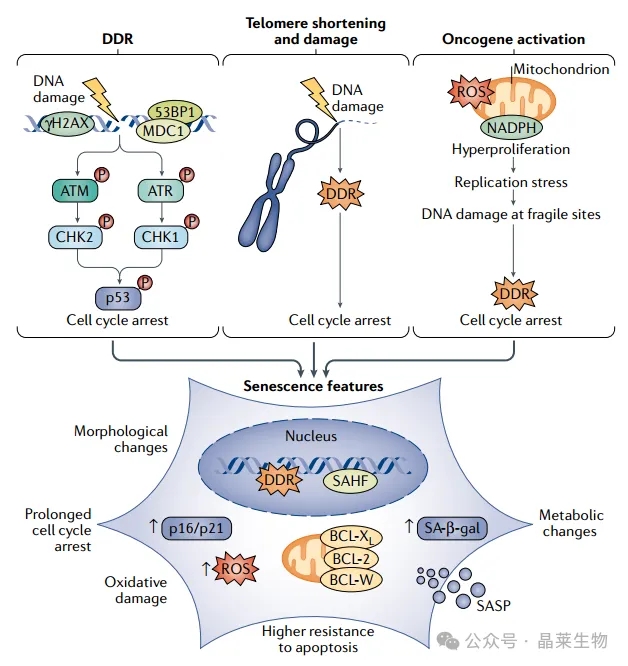
DDR的延长激活会导致衰老。此外,DDR信号在端粒,也就是染色体的末端,也足以引发复制细胞衰老。致癌基因的激活也是一个重要的衰老触发器。大多数激活的癌基因会诱导过度增殖和改变DNA复制模式,这最终会导致复制应激和DNA损伤在脆弱部位,如端粒的积累。
除了DDR的延长激活,衰老的特征还包括细胞周期阻滞(通过p21和p16细胞周期的上调)、氧化损伤(通过ROS水平升高检测)、抗凋亡蛋白BCL-2家族的上调(诱导凋亡抵抗)、代谢变化(包括衰老相关的-β-半乳糖苷酶(SA-β-gal)的积累)、衰老相关的异染色质灶(SAHF)以及衰老相关的分泌表型(SASP)。
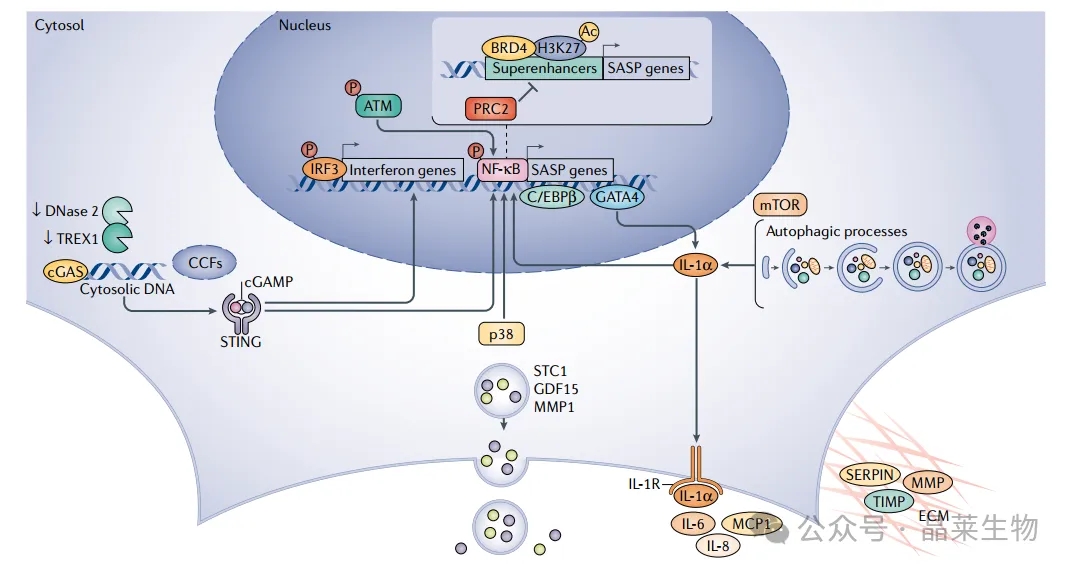
该过程还涉及到一些上游的DNA损伤反应激酶和转录因子,如核因子-κB (NF-κB)和CCAAT/增强子结合蛋白-β (C/EBPβ),它们通过不同的途径诱导SASP基因的激活。
上图描述了表观遗传读取器含溴结构域蛋白4 (BRD4)在SASP基因激活中的作用,它与Polycomb阻遏复合物2 (PRC2)竞争结合乙酰化组蛋白H3 Lys27 (H3K27),从而有助于细胞衰老的正确执行。
上图体现了cGAS-STING通路在SASP程序中的调节作用,该通路能够识别胞质DNA和胞质染色质片段(CCFs),并通过激活NF-κB和干扰素反应因子IRF3来调控SASP基因的表达。此外,cGAS-STING通路的异常激活可能与DNA酶的下调有关,这些酶通常参与细胞质DNA的降解。
高脂肪饮食 (HFD)模型
高脂肪饮食 (HFD) 和肥胖会导致衰老细胞积累并导致多个器官功能受损。例如,HFD诱导的衰老小鼠肾细胞与肾纤维化和功能障碍有关;治疗可减少衰老细胞负荷和 SASP 标志物表达,缓解肾纤维化并改善肾功能。口服酪氨酸激酶抑制剂达沙替尼+天然类黄酮槲皮素可减轻HFD喂养的小鼠的肝脏中衰老肝细胞和肝脂肪变性的负担。
肥胖还会导致小鼠大脑第三脑室附近衰老细胞的积累,以及神经精神功能障碍的发展,特别是焦虑,这是由于位于第三脑室附近的边缘系统功能改变所致。口服酪氨酸激酶抑制剂达沙替尼+天然类黄酮槲皮素可减少这种神经炎症,增加神经发生标志物,减少神经胶质增生并减轻肥胖小鼠的焦虑。
衰老细胞执行不同的生物学功能,这些功能可能以环境依赖的方式产生有害或有益的后果。
1. 组织再生和胚胎发育:通过分泌FGF4和FGF8,引导胚胎瞬时结构中的组织再生和胚胎发育,并通过基质金属蛋白酶2和9 (MMP2和MMP9)塑造胎盘的结构和功能。衰老细胞还通过限制细胞过度增殖来限制组织损伤,并部分通过分泌PDGF-AA来促进伤口愈合。
2. 抑制肿瘤:衰老细胞通过上调p53、p16和p21来自主阻断细胞周期进程,并通过分泌白细胞介素-6 (IL-6)和IL-8来促进邻近细胞的衰老,从而限制肿瘤的发展。
3. 促进促炎微环境的形成:通过分泌白细胞介素-6 (IL-6)、IL-8等炎症因子,支持邻近细胞的衰老和肿瘤的发展。此外,衰老细胞还能分泌多种衰老相关分泌表型(SASP)成分,如IL-6、IL-1受体拮抗剂(IL-1RA)、GROα和干扰素-γ (IFNγ)等,这些成分可以促进无菌慢性炎症的发生和发展。这些炎症因子和SASP成分可能会进一步破坏组织结构,促进炎症和肿瘤的发生。
4. 干预组织的再生能力:当干细胞或祖细胞进入衰老状态时,由于细胞周期抑制蛋白(如p16和p21)的上调,这些细胞无法再发挥支持组织提供新细胞的功能,从而限制了组织的再生能力。同时,衰老细胞还可能通过分泌某些因子促进重编程到胚胎状态,这在一定程度上有利于组织再生,但同时也可能有利于肿瘤的发展。
综上所述,细胞衰老的生物学后果具有复杂性和多样性,既可能带来有益的影响,也可能导致有害的后果。因此,在研究和应用细胞衰老的过程中,需要综合考虑其不同的生物学功能和后果,以实现更好的应用效果。
晶莱生物
以上部分数据与结果图来源于网络和文献,如有侵权请联系客服删除。
关于晶莱
关注公众号,了解更多!